

分析 (1)氧化还原反应中,化合价升高的元素在反应中被氧化,根据电子守恒确定转移电子的量与二氧化硫的量之间的关系;
(2)浓硫酸和亚硫酸钠反应生成二氧化硫,含有水蒸气,通过浓硫酸干燥后通过催化剂的玻璃管,发生反应生成三氧化硫,进入装置D冷却得到三氧化硫,最后通过足量的硝酸钡溶液吸收过滤的二氧化硫,
①根据分液漏斗的使用方法来回答;
②氯酸钾受热分解可以获得氧气;
③为确保实验的准确度,要保证二氧化硫和三氧化硫的量的测定准确;
④根据质量守恒以及转化率=$\frac{消耗量}{起始量}$×100%来计算;
(3)①二氧化硫具有氧化性,可以和最低价的硫化钠发生氧化还原反应;
②氯气具有氧化性,可以将二氧化硫氧化到最高价的硫酸;
③根据溶液中的电荷守恒来回答.
解答 解:(1)氧化还原反应4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$8SO2+2Fe2O3中,化合价升高的Fe、S元素在反应中被氧化,该反应生成8mol的二氧化硫,转移电子的物质的量为44mol,所以当该反应转移2.75mol电子时,生成的二氧化硫的物质的量为0.5mol,在标准状况下的体积为11.2L,故答案为:Fe、S;11.2;
(2)①分液漏斗的使用方法:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加,故答案为:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加;
②氯用图2所示装置制取氧气,即加热固体的方法制氧气,可以让氯酸钾在二氧化锰催化下受热分解获得氧气,方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,
故答案为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
③为确保实验的准确度,要保证二氧化硫和三氧化硫的量的测定准确,当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,可以让装置中的二氧化硫和三氧化硫充分被后面的装置吸收,故答案为:使残留在装置中的二氧化硫和三氧化硫被充分吸收;
④装置D增加的质量为mg,及生成三氧化硫的质量是mg,物质的量是$\frac{mg}{80g/mol}$,装置E中产生白色沉淀的质量为ng,则吸收的二氧化硫的物质的量是$\frac{ng}{233g/mol}$,则二氧化硫的转化率=$\frac{\frac{m}{80}}{\frac{m}{80}+\frac{n}{233}}$×100%,
故答案为:$\frac{\frac{m}{80}}{\frac{m}{80}+\frac{n}{233}}$×100%;
(3)①二氧化硫具有氧化性,可以和最低价的硫化钠发生氧化还原反应,生成淡黄色的沉淀S,故答案为:试管a中出现淡黄色浑浊;
②方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成,可能是氯水中的氯离子产生的作用,
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去,可以是氯水中含有的漂白性物质次氯酸起的作用;
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀,证明溶液汇总出现硫酸根离子,是二氧化硫在酸性环境下和氯水反应生成的,即SO2+Cl2+2H2O=4H++SO42-+2Cl-,
Ⅲ合理,二氧化硫被氧化生成硫酸根离子,和钡离子反应生成白色沉淀,据此能证明二氧化硫的还原性;氯气和二氧化硫 发生氧化还原反应生成硫酸和盐酸,离子方程式为:SO2+Cl2+2H2O=4H++SO42-+2Cl-,
故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;
③将二氧化硫通入到盛有氢氧化钠的试管c中,所得溶液中存在电荷守恒:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),溶液显示中性,所以c(H+)=c(OH-),此时:c(Na+)=2c(SO32-)+c(HSO3-),
故答案为:2c(SO32-)+c(HSO3-).
点评 本题考查了二氧化硫性质应用和实验验证,实验设计的步骤和实验方案的确定应根据题干要求分析判断,关键是读懂题干信息,依据题干条件计算判断,题目较难.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
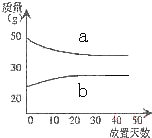
| A. | a挥发、b吸水 | B. | a升华、b冷凝 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
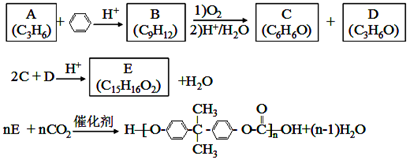
 ;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚.
;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚.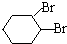 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$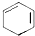 +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+Na+HCO3- Cl- | B. | K+ Na+ HCO3-AlO2- | ||
| C. | Mg2+ NH4+ SO42-Cl- | D. | Fe2+ Na+Cl- NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 88g乙酸乙酯中存在的共价键总数为14NA | |
| C. | 加热时,含2molH2SO4的浓硫酸与足量铜反应,转移的电子数为2NA | |
| D. | 1mol羟基所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠浮在水面上 | B. | 钠熔化成小球并在水面上游动 | ||
| C. | 有无色无味的气体生成 | D. | 水溶液变为红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com