
分析 某有机物A在标况下的密度为1.34g/L,摩尔质量为:1.34g/L×22.4L/mol=30g/mol,而取A与氧气反应,得到等物质的量的CO2和H2O,分子中C、H原子数目之比为1:2,结合相对分子质量为30,可知A的分子式为CH2O.
解答 解:某有机物A在标况下的密度为1.34g/L,摩尔质量为:1.34g/L×22.4L/mol=30g/mol,而取A与氧气反应,得到等物质的量的CO2和H2O,分子中C、H原子数目之比为1:2,结合相对分子质量为30,可知A的分子式为CH2O,作核磁共振氢谱,发现只有一种吸收峰,说明是甲醛,其结构简式为 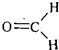 ,结构简式为HCHO,
,结构简式为HCHO,
故答案为:CH2O;HCHO.
点评 本题考查有机物分子式与结构的确定,试题基础性强,贴近高考,有助于培养学生推理能力,注意掌握常见有机物结构与性质.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水蒸气凝结为液态的水 | B. | 氨气和氯化氢反应生成氯化铵晶体 | ||
| C. | 碳酸氢铵在常温情况下分解 | D. | CO点燃时生成CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
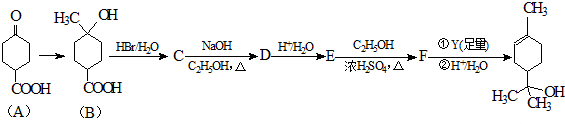
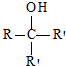
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
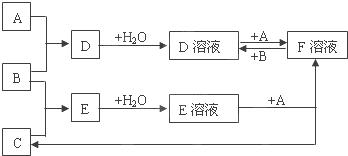
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
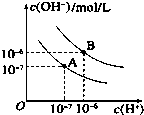 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;点燃\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | 向Na2SiO3溶液中加入盐酸:Na2SiO3+2H+═H2SiO3(胶体)+2Na+ | |
| C. | 向 溶液中通入少量CO2:2 溶液中通入少量CO2:2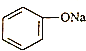 +H2O+CO2→2 +H2O+CO2→2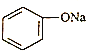 +CO32- +CO32- | |
| D. | 向Mg(OH)2悬浊液中加入饱和NH4Cl溶液:2NH4++Mg(OH)2═2NH•H2O+Mg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com