
| 加入的物质 | 结论 | |
| A | 50mL 1mol/L H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.5mol CaO | 若反应完全后溶液的体积仍为100mL,则溶液的pH约为14 |
| C | 50mL H2O | c(Na+)=2[c(CO32-)+c(HCO3-)] |
| D | 0.1mol NaHSO4 | 反应完全后,溶液pH减小,c (Na+)不变 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.n(H2SO4)=1mol/L×0.05L=0.05mol,二者恰好完全反应生成硫酸钠和二氧化碳、水,根据物料守恒判断;
B.CaO和水反应生成氢氧化钙,二者反应生成CaCO3沉淀和NaOH,根据Na原子守恒得n(NaOH)=2n(Na2CO3)=2×0.05mol=0.1mol,溶液中c(NaOH)=$\frac{0.1mol}{0.1L}$=1mol/L;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.加入0.1mol硫酸氢钠,二者恰好反应生成硫酸钠、水和二氧化碳,硫酸氢钠能电离出钠离子而导致溶液中c(Na+)增大.
解答 解:A.n(H2SO4)=1mol/L×0.05L=0.05mol,二者恰好完全反应生成硫酸钠和二氧化碳、水,根据物料守恒得c(Na+)=2c(SO42-),故A错误;
B.CaO和水反应生成氢氧化钙,二者反应生成CaCO3沉淀和NaOH,根据Na原子守恒得n(NaOH)=2n(Na2CO3)=2×0.05mol=0.1mol,溶液中c(NaOH)=$\frac{0.1mol}{0.1L}$=1mol/L,溶液的pH=14,故B正确;
C.任何电解质溶液中都存在物料守恒,根据物料守恒得c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故C错误;
D.加入0.1mol硫酸氢钠,二者恰好反应生成硫酸钠、水和二氧化碳,硫酸氢钠能电离出钠离子而导致溶液中c(Na+)增大,溶液的pH减小,故D错误;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断及计算能力,明确物质之间的反应、溶液中溶质成分及其性质是解本题关键,注意电荷守恒和物料守恒的正确运用,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则b=a+1 | |
| B. | 某溶液由水电离的c(OH-)=1.0x10-13mol/L,则此溶液一定显酸性 | |
| C. | 将pH=4的醋酸稀释1000倍,溶液的pH=7 | |
| D. | pH=13的强碱溶液和pH=2的强酸溶液混合,若所得溶液的pH=7,则强碱与强酸的体积比是1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
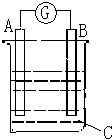 请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,
请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com