
| A. | 用润湿的pH试纸测稀碱溶液的pH,测定值偏小 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏大 | |
| C. | 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏大 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
分析 A.湿润的pH值试纸将碱液稀释,氢氧根离子浓度减小;
B.定容时俯视刻度线,导致溶液的体积偏小;
C.滴定前滴定管内无气泡,终点读数时有气泡,气体占据液体应占有的体积;
D.测定中和热时应迅速加入碱液,防止热量散失.
解答 解:A.用润湿的pH试纸测稀碱溶液的pH相当于对待测液进行了稀释,浓度变小,碱性减弱,测定的pH减小,故A正确;
B.俯视时读的是真实值的上方刻度,定容时俯视刻度线,水并没有加到刻度线,导致溶液体积偏小,所得溶液的浓度偏大,故B正确;
C.滴定前滴定管内无气泡,终点读数时有气泡,气体占据液体应占有的体积,会导致所测溶液体积偏小,故C错误;
D.碱缓慢倒入酸中,不能准确测定反应的最高温度,热量损失导致所测温度值偏小,应一次性迅速将将碱倒入酸中,故D正确;
故选C.
点评 本题考查较为综合,涉及pH试纸的使用、溶液配制、中和滴定、中和热测定等知识,题目难度中等,明确常见化学实验基本操作方法即可解答,试题有利于提高学生的分析能力及化学实验能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y<Z<W | |
| B. | 原子最外层电子数:W>Z>Y | |
| C. | X、Y可以形成既有极性键也有非极性键的化合物 | |
| D. | 由X、Y、Z三种元素形成的化合物的水溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高压钠灯能发出透雾能力强的淡紫色光,常用做路灯 | |
| B. | 用水清洗盛装过浓硫酸的铁捅要远离火源 | |
| C. | 理电池应用广泛,是因为锉能直接与水反应,不需要特殊的电解质溶液 | |
| D. | 据报导,一定条件下氢气可转变为金属氢,金属氢具备超导等优良性能.由氢气转变为金属氢属于同一元索的同位素之间的转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 LpH=l Ba(OH)2溶液中所含OH-的数目为0.2NA | |
| B. | 28g聚乙烯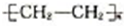 中含有的碳原子数为2NA 中含有的碳原子数为2NA | |
| C. | 1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的数目为NA | |
| D. | 1 mol Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基(CH3-)所含的电子数为10NA | |
| B. | 46g由NO2和N2O4组成的混合气体中,含有的原子总数为3NA | |
| C. | 常温常压下,1mol分子式为C2H6O的有机物中,含有C-O键的数目为NA | |
| D. | 标准状次下产22.4L四氯化碳中含有C-Cl键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
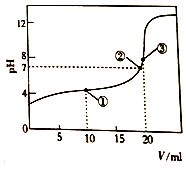 298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )
298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )| A. | HR溶液中只含有一种分子和三种离子 | |
| B. | 在①②③点对于的溶液中,②点水的电离程度最大 | |
| C. | ③点对应的溶液中有c(R-)>c(Na+)>c(H+)>c(OH-) | |
| D. | ①点对应的溶液中R-的水解程度小于HR的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H2R是二元弱酸,其Ka1=1×10-2 | |
| B. | NaHR在溶液中水解程度小于电离程度 | |
| C. | pH<7.2的溶液中一定存在:c( Na+)>c( HR-)>c(R2-)>c(H+)>c(OH-) | |
| D. | 含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com