
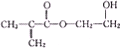 甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )
甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )| A、能发生加成反应 |
| B、能发生取代反应 |
| C、一定条件下,能与乙醇发生酯化反应 |
| D、既能是溴水褪色,又能使酸性高猛酸钾溶液褪色 |


科目:高中化学 来源: 题型:
| 实验变量 实验序号 | 银氨溶液量 (ml) | 乙醛的量 (滴) | 水浴温度 (℃) | 反应混合液PH | 出现银镜时间(min) |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2 (g)+O2(g)=2H2O(g)△H1 2H2(g)+O2 (g)=2H2O(l)△H2 | ||||
| B、S(s)+O2(g)=SO2 (g)△H1 S(g)+O2(g)=SO2 (g)△H2 | ||||
C、CO(g)+
| ||||
D、H2 (g)+Cl2 (g)=2HCl(g)△H1
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、NaOH溶液的物质的量浓度为0.1mol/L |
| B、P点时反应恰好完全中和,溶液pH为7 |
| C、曲线a是NaOH人滴定盐酸的滴定曲线 |
| D、P点时溶液中的离子浓度为c(Na+)=c(Cl-)=c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素B位于元素周期表中第三周期ⅣA族 |
| B、在元素A所在的主族元素的最简单氢化物中,A的氢化物最稳定 |
| C、元素A与元素B形成的化合物在工业上可用作制玻璃的原料 |
| D、元素A与元素B形成的化合物遇任何酸都不能反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、价层电子构型为7S2 |
| B、单质能与冷水反应,放出氢气 |
| C、氢氧化物呈两性 |
| D、碳酸盐难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2能使溴水、酸性高锰酸钾溶液退色是因为SO2有漂白性 |
| B、若将SO2和Cl2以等物质的量混合后通入品红溶液中一定退色更快 |
| C、SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀全部溶解 |
| D、SO2通入BaCl2溶液中无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁合金为电源负极,发生氧化反应 |
| B、电解质溶液中的H+向正极移动 |
| C、正极反应为:H2O2+2e-=2OH- |
| D、放电时正极周围溶液的pH升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com