
【题目】实验室有一瓶久置的Na2SO3固体试剂,已部分变质,为测定其纯度,实验设计与操作如下,请回答问題:
(1)Na2SO3变质的原因(用化学方程式表示)___________。
(2)取一定量的样品溶于水,加入过量的BaCl2溶液,然后过滤(如图)、洗涤、干燥、称量,其中洗涤沉淀的具体操作为___________。
(3)实验时用BaCl2比用CaCl2好,写出两点理由:___________。
【答案】 2Na2SO3+O2=2Na2SO4 用玻璃棒引流,往漏斗中加入蒸馏水,浸没沉淀物,让水自然流下,重复2~3次 一是用BaCl2作沉淀剂,BaSO4、BaSO3的相对分子质量大,生成沉淀质量大,称量误差小;二是用CaCl2作沉淀剂,CaSO4微溶,有误差。
【解析】(1)本题考查Na2SO3的性质,Na2SO3中S显+4价,以还原性为主,容易被氧气氧化成Na2SO4,即化学反应方程式为2Na2SO3+O2=2Na2SO4;(2)考查实验基本操作,洗涤沉淀的方法是:用玻璃棒引流,往漏斗中加入蒸馏水,浸没沉淀物,让水自然流下,重复2~3次;(3)考查沉淀剂的选择,用BaCl2作沉淀剂,因为Ba的相对原子质量大于Ca,因此有BaSO4、BaSO3的相对分子质量大,生成沉淀质量大,称量误差小;用CaCl2作沉淀剂,CaSO4微溶,有误差。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知NH4CuSO3与足量的1mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色,据此判断下列说法合理的是
A.NH4CuSO3中硫元素被氧化 B.该反应表明硫酸具有酸性
C.刺激性气味的气体是氨气 D.该反应中硫酸作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 澄清石灰水中加盐酸:2H++Ca(OH)2===Ca2++2H2O
B. 向NaHCO3溶液中加入NaOH溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 氯气溶于水:Cl2+H2O![]() 2H++ClO-+Cl-
2H++ClO-+Cl-
D. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO![]() ===BaSO4↓+H2O
===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 次氯酸钠溶液中通入过量的二氧化硫:ClO-+SO2+H2O===HSO![]() +HClO
+HClO
B. 等物质的量浓度、等体积的硫酸氢钠溶液和氢氧化钡溶液反应:H++SO![]() +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
C. 氯气和水的反应:Cl2+H2O===2H++Cl-+ClO-
D. 向碳酸氢钾溶液中滴入过量澄清石灰水:2HCO![]() +Ca2++2OH-===CO
+Ca2++2OH-===CO![]() +2H2O+CaCO3↓
+2H2O+CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 钠与水反应:Na+2H2O===Na++2OH-+H2↑
B. 硫酸铜溶液与氢氧化钡溶液反应:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. 碳酸钙与稀盐酸反应:CO![]() +2H+===H2O+CO2↑
+2H+===H2O+CO2↑
D. 向FeCl3溶液中加入氨水:Fe3++3NH3·H2O===Fe(OH)3↓+3NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为冰晶石(化学式为Na3AlF6)的晶胞。己知冰晶石熔融时电离方程式为:Na3AlF6![]() 3Na++AlF63-。图中●位于大立方体顶点和面心,○位于大立方体的12 条棱的中点和8个小立方体的体心。则下列说法正确的是( )
3Na++AlF63-。图中●位于大立方体顶点和面心,○位于大立方体的12 条棱的中点和8个小立方体的体心。则下列说法正确的是( )
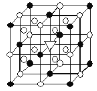
A. 冰晶石是原子晶体 B. 该物质中存在配位键
C. 大立方体的体心处△代表的是Al3+ D. 该物质是电解冶炼铝的还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定被还原的氯元素与被氧化的氯元素的物质的量之比为3∶1,则Cl2与NaOH溶液反应时,所得溶液中Cl-与ClO![]() 的物质的量浓度之比为( )
的物质的量浓度之比为( )
A. 21∶5 B. 1∶1 C. 6∶1 D. 4∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com