
| ������ |
| ��ʼ�� |
| c(H2)?c?(CO2) |
| c(CO)?c(H2O) |
| X2 |
| (0.01-X)2 |
| 0.0075 |
| 0.01 |


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��X��Y��Z��W��ԭ�Ӱ뾶�Ĵ�С��ϵΪ��W��Y��Z��X |
| B���ڻ�����Y2X2��Z2X4��X2W2�У����������Ĺ��õ��Ӷ������ |
| C����Ԫ��Y��Z��ȣ�Ԫ��W�γɵļ��⻯�����ȶ�������Ϊ����Ӽ������� |
| D��X��Y��Z��W����Ԫ�ؿ��γɻ�ѧʽΪX7Y2ZW2�Ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
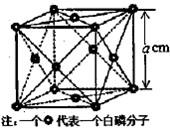 ����Ԫ�ذ���N��P��As��Sb��Bi����Ԫ�أ�
����Ԫ�ذ���N��P��As��Sb��Bi����Ԫ�أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���Բ��ϵ��������Ͻ����Fe��NO3��3��Ni��NO3��2������ͪ뿡��������������������ơ������������һ�������·�Ӧ�Ƶã�
���Բ��ϵ��������Ͻ����Fe��NO3��3��Ni��NO3��2������ͪ뿡��������������������ơ������������һ�������·�Ӧ�Ƶã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�����ģ�ʡ�Լг�װ�ã� | ��Ӧʵ�� | |
| A | �ձ����������������� | ���ؽᾧ�����ᴿ��NaCl���ʵ�KNO3 |
| B | �ձ�������������ͷ�ι� | ��ϡ�����ȥ�Ȼ����е������Ȼ����� |
| C | �ձ�������������ͷ�ιܡ���Һ©�� | ����ˮ��CCl4��ȥKCl��Һ�е�����KI |
| D | �ձ�������������ͷ�ιܡ�����ƿ | ��Ũ��������500mL 0.1mol/L����Һ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������pHΪ5��������Һϡ��1000����pH����8 |
| B��̼������Һ�д��ڣ�c��Na+��+c��H+��=c��CO32-��+c��OH-��+c��HCO3-�� |
| C��Ũ�Ⱦ�Ϊ0.1mol/L�İ�ˮ���Ȼ����Һ��ˮ�������c��H+��ǰ��С�ں��� |
| D����Ũ�ȵ�CH3COOH��KOH������Ȼ�ϣ�c��K+��+c��H+��=c��OH-��+c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��N2�Ľṹʽ N��N |
B��Cl-�Ľṹʾ��ͼ |
C��CO2�ĵ���ʽ |
D���õ���ʽ��ʾHCl���γɹ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com