
 ,则CH3+的电子式为
,则CH3+的电子式为 ,其中CH3+中碳是sp2杂化,所以键角为 120°,故答案为:
,其中CH3+中碳是sp2杂化,所以键角为 120°,故答案为: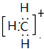 、
、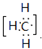 、120°;
、120°; ,
, .
.


科目:高中化学 来源: 题型:
| A、增加气体反应物的浓度可以提高活化分子百分数 |
| B、升高温度可增加单位体积活化分子数 |
| C、发生有效碰撞的分子一定是活化分子 |
| D、使用催化剂可降低活化能,提高单位体积活化分子百分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积:①④③② |
| B、密度:④①②③ |
| C、质量:①④③② |
| D、氢原子数:①③④② |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
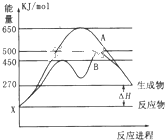 (1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
(1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 铝和氢氧化钾都是重要的工业产品.请回答:
铝和氢氧化钾都是重要的工业产品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
 某化合物的结构示意图如右,下列关于该化合物的叙述中正确的是( )
某化合物的结构示意图如右,下列关于该化合物的叙述中正确的是( )| A、该化合物只含有H、N、O、Ni四种元素 |
| B、该化合物是配合物,中心离子的配位数是2,配体是氮元素 |
| C、该化合物属于配合物,中心离子是Ni离子 |
| D、该化合物不属于配合物,而是属于高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com