
| A. | ①② | B. | ①③ | C. | ④⑤ | D. | ②④ |
分析 含有孤电子对和含有空轨道的原子之间易形成配位键,据此判断含有配位键的物质.
解答 解:含有孤电子对和含有空轨道的原子之间易形成配位键,
①H3O+中氢离子存在空轨道、O原子存在孤电子对,所以该微粒中含有配位键,故正确;
②[Cu(NH3)4]2+中Cu原子含有空轨道、N原子含有孤电子对,所以该微粒中含有配位键,故正确;
③CH3COO-中不存在含有空轨道的原子,所以不存在配位键,故错误;
④NH3中N原子含有孤电子对,没有含有空轨道的原子,所以该微粒中不存在配位键,故错误;
⑤CH4中没有含有空轨道和孤电子对的原子,所以该微粒中不存在配位键,故错误;
故选A.
点评 本题考查配合物成键情况,明确配合物构成条件是解本题关键,注意配位键属于共价键,题目难度不大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题
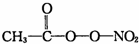 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
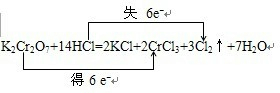
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L | |
| B. | 制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况) | |
| C. | 0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023 | |
| D. | 10g 98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol SO42-的质量是96 g | B. | 1mol H2O的质量是18 g/mol | ||
| C. | CO2的摩尔质量是44 g | D. | HCl的相对分子质量是36.5 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 属于金属元素 | |
| B. | 质子数与中子数之差为50 | |
| C. | 原子的核外电子数是39 | |
| D. | ${\;}_{39}^{49}$Y和${\;}_{39}^{50}$Y是两种不同的核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
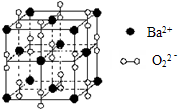
| A. | 该氧化物是含有非极性键的离子化合物 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该晶体晶胞结构与CsCl相似 | |
| D. | 晶体中Ba2+的配位数为8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com