

分析 (1)锌和浓硫酸反应是二氧化硫、硫酸锌和水;
(2)装置是气体验证试验,所以需要装置气密性完好;
(3)二氧化硫具有漂白性,通常用品红溶液检验二氧化硫的存在;E作用为防止空气中进入D,可以选择碱石灰;
(4)氢气具有还原性能够还原氧化铜,水与无水硫酸铜生成蓝色的五水硫酸铜;
(5)B装置的作用是吸收水,防止后面的氢气的检验.
解答 解:(1)锌和浓硫酸反应是二氧化硫、硫酸锌和水,反应的化学方程式为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O,
故答案为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O;
(2)装置是气体验证试验,所以需要装置气密性完好,实验开始先检验装置的气密性,
故答案为:检查装置的气密性;
(3)二氧化硫具有漂白性,通常用品红溶液检验二氧化硫的存在;E作用为防止空气中进入D,可以选择碱石灰;
故答案为:品红溶液;碱石灰;
(4)氢气具有还原性能够还原氧化铜,所以若有氢气则C装置中黑色氧化铜变为红色铜,D装置中白色硫酸铜变为蓝色;
故答案为:黑色的CuO变成红色的Cu;D装置中白色硫酸铜变为蓝色;
(5)锌和硫酸反应生成的气体中必含有水,如果去掉装置B,因为混合气体中含有的H2O会干扰H2的检验,
故答案为:不能;因为混合气体中可能含有H2O会干扰H2的检验.
点评 本题考查锌和硫酸的反应及产物的检验,注意掌握浓硫酸的性质,根据需检验气体的性质、检验方法理解检验的先后顺序是解答的关键,题目难度中等.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:解答题
| I A | IIA | ⅢA | IVA | VA | ⅥA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
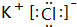
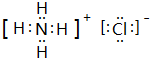 ,M中的化学键类型为离子键、共价键.
,M中的化学键类型为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
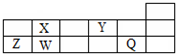
| A. | W、X两元素在自然界中都存在相应的单质 | |
| B. | Q、Y分别与钠元素形成的化合物中仅含离子键 | |
| C. | 简单离子半径由大到小的顺序为:Q>Y>Z | |
| D. | X、Z的最高价氧化物对应的水化物之间易发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生利用物质间的互变,设计成一个平面魔方,如图所示:
某学生利用物质间的互变,设计成一个平面魔方,如图所示:| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色(粉末状时为黑色)黄色红 | 褐色 | 红棕色 | 浅绿色 |
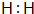 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
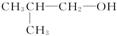
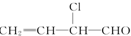
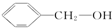
| A. | ②③⑤ | B. | ②④⑥ | C. | ③④⑥ | D. | ①②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
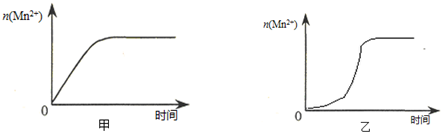
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com