
下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图。

在上述实验过程中,所涉及的三次分离操作分别是
A.①蒸馏、②过滤、③分液 B.①分液、②蒸馏、③蒸馏
C.①蒸馏、②分液、③分液 D.①分液、②蒸馏、③结晶、过滤
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是( )
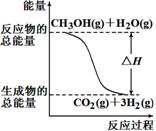
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是
A. 反应①中的能量变化如右图所示
B. 可推知2H2(g)+O2(g)=2H2O(g)
ΔH=-483.8 kJ/mol
C. 1 mol CH3OH充分燃烧放出的热量为192.9 kJ
D. CH3OH转变成H2的过程一定要吸收能量
查看答案和解析>>
科目:高中化学 来源: 题型:
在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学原子经济要求的是
A. 乙烯聚合为聚乙烯高分子材料 B. 甲烷与氯气制备一氯甲烷
C. 以铜和浓硝酸为原料生产硝酸铜 D. 用二氧化硅制备高纯硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中,不管以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳物质的量不变的是
A.乙烯(C2H4)和乙炔(C2H2) B.乙醇和丙醇(CH3CH2CH2OH)
C.乙醇和乙醚(C2H5OC2H5) D.甲醛( HCHO)和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方法中可以证明2HI(气) H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是
① 单位时间内生成n mol H2的同时生成n mol HI
② 一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④ 反应速率υ(H2)=υ(I2)=0.5υ(HI)时
⑤ c(HI)=c(H2)=c(I2)=2:1:1
⑥ 温度和体积一定时,某一生成物浓度不再变化
⑦ 温度和体积一定时,容器内压强不再变化
⑧ 条件一定,混合气体的平均相对分子质量不再变化
⑨ 温度和体积一定时混合气体的颜色不再变化
A. ②③④⑤⑥ B. ②⑥⑦⑧⑨ C. ①②⑥⑧ D. ②⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是___________________
 负极反应式为:______________________________。
负极反应式为:______________________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为____________________________________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为
 Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
①该电池工作时,b口通入的物质为_______,
c口通入的物质为______。
②该电池负极的电极反应式为:_______
③工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有______________NA个电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释 ④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥食物腐败
A.②③④⑤⑥ B.②③④ C.②⑤⑥ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L的Fe2(SO4)3溶液中Fe3+的浓度为0.2mol/L,与0.2L0.5mol/L的Na2SO4溶液中SO42-的浓度之比是( )
A.3:2 B.2:5 C.3:5 D.5:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com