
【题目】某兴趣小组在实验室模拟反应![]() 制备重要的化工原料
制备重要的化工原料![]() 。
。
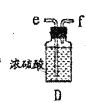
已知:![]() 熔点-93.6℃,沸点76.1℃,遇水极易水解,易与
熔点-93.6℃,沸点76.1℃,遇水极易水解,易与![]() 反应;
反应;![]() 熔点1.25℃,沸点105.8℃,遇水强烈水解,能溶于
熔点1.25℃,沸点105.8℃,遇水强烈水解,能溶于![]() 。
。
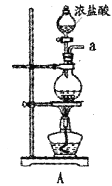
(1)装置A中发生反应的离子方程式是__________________。
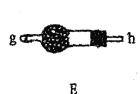
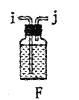
(2)以上各仪器接口的连接顺序是a→____→____→____→____→cd←g←h←b,装置E中的试剂为无水氯化钙,F中所装的试剂是________。(仪器不重复使用)
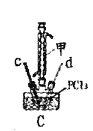
(3)装置C制备![]() 。
。
①仪器甲的名称是_______。
②反应温度控制在60~65℃,其原因是______________。
③![]() 发生水解反应生成
发生水解反应生成![]() 和_____________。
和_____________。
(4)该装置不足之处是_____________。
【答案】4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O i j e f 饱和食盐水 球形冷凝管 温度太低,反应速率太慢;因为
Mn2++Cl2↑+2H2O i j e f 饱和食盐水 球形冷凝管 温度太低,反应速率太慢;因为![]() 沸点是76.1℃,温度太高
沸点是76.1℃,温度太高![]() 、
、![]() 挥发 SO2 缺少尾气处理装置
挥发 SO2 缺少尾气处理装置
【解析】
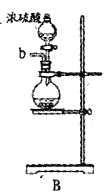
A装置制备氯气,其中混有氯化氢和水蒸气,需要经过F装置中饱和食盐水除去氯化氢,通过D装置的浓硫酸干燥,再通入C中,由装置B制取二氧化硫,需通过E中干燥剂干燥后在通入C中反应,加热条件下发生PCl3+SO2+Cl2![]() POCl3+SOCl2,以此解答。
POCl3+SOCl2,以此解答。
(1)A用于制备氯气,发生反应的离子方程式为4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)由以上分析可知连接顺序为a→i→j→e→f→cd←g←h←b,E应盛放固体干燥剂,F用于除去氯气中的氯化氢,可用饱和食盐水(或饱和NaCl溶液);
(3)①由仪器的结构和性能可知仪器甲为冷凝管;
②B中反应温度控制在60~65℃,因为温度过高,PCl3、SO2会大量挥发,导致产量降低,温度过低,反应速率会变慢;
③SOCl2发生水解反应生成二氧化硫和盐酸,化学方程式是SOCl2+H2O=SO2↑+2HCl;
(4)含有SO2的尾气对环境有污染,需要添加尾气处理装置。


科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟工业制漂白粉,设计了如下图所示的实验装置。
已知:①氯气与碱反应放出热量。②6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。
试回答下列问题:

(1)甲装置中仪器a的名称是________________________。
(2)装置乙中饱和食盐水的作用是________________________。
(3)装置丁中发生反应的化学方程式为_____________________。
(4)漂白粉在空气中失效的原因是______________、______________(用化学方程式表示)。
(5)①该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是________ 。
②为提高Ca(ClO)2的含量。可采取的措施是___________(任写一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到密度为1.15g/cm3的混合溶液。计算(写出计算步骤):
(1)混合后溶液的质量分数;______________
(2)混合后溶液的物质的量浓度;(保留到小数点后一位,下同)___________
(3)在1 000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A. 溶液中![]() 不变
不变
B. 溶液中导电粒子的数目减少
C. 醋酸的电离程度增大,c(H+)也增大
D. 再加入10 mL pH=11的NaOH溶液后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷的单质及其化合物用途非常广泛。完成下列填空:
(1)画出磷的原子结构示意图________。
(2)磷酸钙真空制磷的反应为![]() 。该反应的氧化产物是________(填化学式);
。该反应的氧化产物是________(填化学式);![]() 中的共价键的类型为________。
中的共价键的类型为________。
(3)次磷酸钠的结构为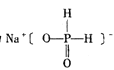 。
。
①次磷酸钠的化学式为________,磷的化合价为________。
②次磷酸钠为________盐(填“正”“酸式”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置中, a、b为石墨电极,通电一段时间后,b极附近显红色。下列说法不正确的是
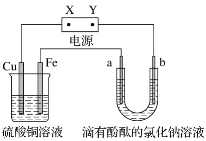
A. b电极反应式为2H++2e-=H2↑B. a电极反应式为2Cl--2e-=Cl2↑
C. 铁电极反应式为Cu2++2e-=CuD. 铜电极反应式为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】面对全球近期的气候异常,环境问题再次成为焦点。SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径。
(1)已知:H2O(g)=H2O(l) ΔH1=-Q1 kJ/mol
C2H5OH(g)=C2H5OH(l) ΔH2=-Q2 kJ/mol
C2H5OH(g)+3O2(g)=2CO2 (g)+3H2O(g) ΔH3=-Q3 kJ/mol
则23g液态酒精完全燃烧并恢复至室温放出的热量为________________kJ。
(2)下表为反应2SO2(g)+O2 (g)![]() 2SO3(g)的相应温度下平衡常数的数值,由此得出该反应的ΔH__________0(填“>”“=”或“<”)。
2SO3(g)的相应温度下平衡常数的数值,由此得出该反应的ΔH__________0(填“>”“=”或“<”)。
T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 2.6 | 1.9 | 1.0 | 0.7 | 0.6 |
(3)①已知:在2L密闭容器中,17℃、1.01×105Pa条件下,2NO2(g)![]() N2O4(g) ΔH<0的平衡常数K=13.3。当此反应达到平衡时,若n(NO2)=0.060mol,则c(N2O4)=_______(保留两位有效数字)。
N2O4(g) ΔH<0的平衡常数K=13.3。当此反应达到平衡时,若n(NO2)=0.060mol,则c(N2O4)=_______(保留两位有效数字)。
②若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.040mol/L,c(N2O4)=0.0070mol/L,则改变的条件是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种具有抗疟药理活性的喹啉类衍生物,其合成路线流程图如下:
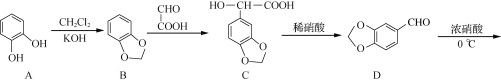
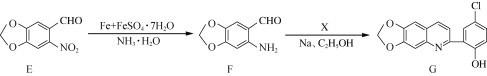
已知: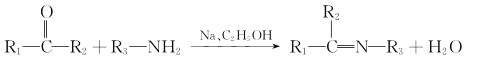
(1) F中的含氧官能团名称为________、________。
(2) B→C的反应类型为________。
(3)芳香族化合物X的分子式为C8H7ClO2,写出X的结构简式:___________________________。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:__________________________。
①分子中含有苯环,能与FeCl3溶液发生显色反应,不能发生银镜反应;
②碱性条件水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢。
(5)写出以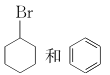 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂和乙醇任用,合成路线流程图示例见本题题干)_________________________。
的合成路线流程图(无机试剂和乙醇任用,合成路线流程图示例见本题题干)_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应3BrF3 + 5H2O = Br2 + HBrO3 + O2↑ + 9HF,当生成3 mol Br2时,被水还原的BrF3的物质的量为
A.9 molB.6 molC.4 molD.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com