
| A. | 1min内用O2表示的反应速率为0.03 mol•L-1•min-1 | |
| B. | 该反应的平衡常数数值为7.5 | |
| C. | SO2的平衡转化率为60% | |
| D. | 降低温度,SO2平衡浓度减小 |
分析 向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,1min后达到平衡,压强变为原来的80%,设转化的氧气为xmol,则
SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)
开始 0.2 0.1 0
转化 2x x 2x
平衡0.2-2x 0.1-x 2x
则$\frac{2x+0.2-2x+0.1-x}{0.2+0.1}$=80%,
解得x=0.03,
A.结合v=$\frac{△c}{△t}$计算;
B.K为生成物浓度幂之积与反应物浓度之积的比,K=;
C.转化率=$\frac{转化的量}{开始的量}$×100%;
D.△H<0,降低温度,平衡正向移动.
解答 解:向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,1min后达到平衡,压强变为原来的80%,设转化的氧气为xmol,则
SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)
开始 0.2 0.1 0
转化 2x x 2x
平衡0.2-2x 0.1-x 2x
则$\frac{2x+0.2-2x+0.1-x}{0.2+0.1}$=80%,
解得x=0.03,
A.1min内用O2表示的反应速率为$\frac{\frac{0.03mol}{2L}}{1min}$=0.015 mol•L-1•min-1,故A错误;
B.K为生成物浓度幂之积与反应物浓度之积的比,K=$\frac{(\frac{2×0.03mol}{2L})^{2}}{(\frac{0.14mol}{2L})^{2}×(\frac{0.07mol}{2L})}$=0.007,故B错误;
C.SO2的平衡转化率为$\frac{转化的量}{开始的量}$×100%=$\frac{2×0.03mol}{0.2mol}$×100%=30%,故C错误;
D.△H<0,降低温度,平衡正向移动,SO2平衡浓度减小,故D正确;
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率计算等为解答的关键,侧重分析与计算能力的考查,注意利用平衡浓度计算K,题目难度不大.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:实验题
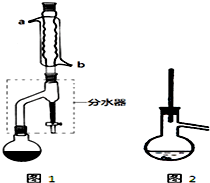 有机物的反应往往伴随副反应发生,因此 需要分离提纯.有一种水果香精的合成步骤如下:
有机物的反应往往伴随副反应发生,因此 需要分离提纯.有一种水果香精的合成步骤如下:| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
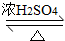 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的原子核外电子层数随质子数的增加而增多 | |
| B. | 它们的L层电子数都相同 | |
| C. | 它们的原子核对最外层电子的引力逐渐减弱 | |
| D. | 它们与氧气或水反应时越来越剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K1=K2 | B. | K1<K2 | C. | K1>K2 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 700 | 830 | 1200 |
| K值 | 1.7 | 1.0 | 0.4 |
| A. | 反应初始至平衡,A的平均反应速率v(A)=0.005 mol•L-1•s-1 | |
| B. | 增大压强,正、逆反应速率均加快 | |
| C. | 该反应正向为吸热反应,升高温度,K值增大,平衡正向移动 | |
| D. | 达到平衡后,B的转化率为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L H2SO4溶液进行中和热的测定:
某实验小组用0.50mol/L NaOH溶液和0.50mol/L H2SO4溶液进行中和热的测定:| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
| 实验次数 温度 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③④ | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{17}O$原子核内含有8个中子 | B. | ${\;}_{8}^{17}O$原子核内含有8个质子 | ||
| C. | ${\;}_{8}^{17}O$原子核外有17个电子 | D. | ${\;}_{8}^{17}O$原子核内含有17个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com