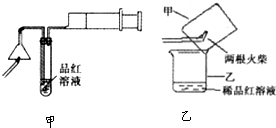
某研究性学习小组进行了Fe(OH)
3胶体的制备:将饱和三氯化铁溶液滴入沸水中时,液体变为
红褐
红褐
色,得到的是
Fe(OH)3胶体
Fe(OH)3胶体
;反应的离子方程式为
.用此分散系进行实验:
(1)将其装入U形管内,用石墨作电极,接通直流电源,通电一段时间后,发现阴极附近颜色
逐渐变深
逐渐变深
,这表明
Fe(OH)3胶粒带正电荷
Fe(OH)3胶粒带正电荷
,这种现象称为
电泳
电泳
.
(2)向其中加入饱和的硫酸铵溶液,发生的现象是
形成红褐色沉淀
形成红褐色沉淀
,原因是
电解质电离出的离子中和了胶体粒子所带电荷,使Fe(OH)3胶体聚沉
电解质电离出的离子中和了胶体粒子所带电荷,使Fe(OH)3胶体聚沉
.
(3)向其中逐滴加入过量稀硫酸,现象是
先出现红褐色沉淀,后沉淀溶解,得棕黄色溶液
先出现红褐色沉淀,后沉淀溶解,得棕黄色溶液
,原因是
电解质使Fe(OH)3胶体聚沉,随着稀硫酸的加入,H+与Fe(OH)3发生反应,Fe(OH)3+3H+═Fe3++3H2O,使沉淀溶解
电解质使Fe(OH)3胶体聚沉,随着稀硫酸的加入,H+与Fe(OH)3发生反应,Fe(OH)3+3H+═Fe3++3H2O,使沉淀溶解
.
(4)提纯此分散系的方法叫
渗析
渗析
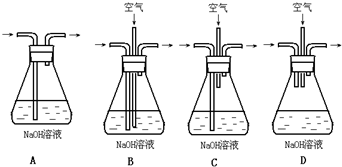
,所选提纯装置是下列中的
E
E
.





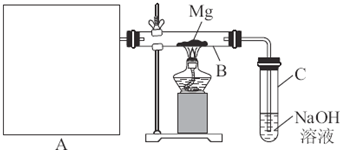


 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).