
【题目】下列离子方程式或化学方程式中正确的有()
①向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
②向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO
③将CO2气体通过过氧化钠固体:2CO2+2Na2O2=2Na2CO3+O2
④将SO2气体通过过氧化钠固体:2SO2+2Na2O2=2Na2SO3+O2
⑤氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO![]() =CaCO3↓+H2O
=CaCO3↓+H2O
⑥在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO![]() =3Fe3++2H2O+NO↑
=3Fe3++2H2O+NO↑
⑦硫酸铁溶液与氢氧化钡溶液反应:Fe3++3OH-=Fe(OH)3↓
A.2项B.3项C.4项D.5项
【答案】A
【解析】
①向次氯酸钙溶液中通入过量CO2应得到碳酸氢钙,则Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO错误;
②向次氯酸钙溶液中通入SO2发生氧化还原反应,则Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO错误;
③将CO2气体通过过氧化钠固体生成碳酸钠和氧气,则2CO2+2Na2O2=2Na2CO3+O2正确;
④将SO2气体通过过氧化钠固体,按氧化还原反应原理,Na2SO3会被O2氧化故不能共存,则2SO2+2Na2O2=2Na2SO3+O2错误;
⑤氢氧化钙溶液与碳酸氢镁溶液反应,除了生成CaCO3和H2O外,会有氢氧化镁沉淀,则Ca2++OH-+HCO![]() =CaCO3↓+H2O错误;
=CaCO3↓+H2O错误;
⑥在氯化亚铁溶液中加入稀硝酸发生氧化还原反应,Fe2+被稀硝酸氧化,则3Fe2++4H++NO![]() =3Fe3++2H2O+NO↑正确;
=3Fe3++2H2O+NO↑正确;
⑦硫酸铁溶液与氢氧化钡溶液反应,Fe(OH)3和硫酸钡沉淀,则Fe3++3OH-=Fe(OH)3↓错误;
则一共有2项正确;
答案选A。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】A、B、C均为短周期元素,它们在周期表中的位置如图。已知B、C两元素在周期表中族序数之和是A元素序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组是( )
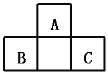
A.Be、Na、AlB.B、Mg、SiC.O、P、ClD.C、Al、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫—碘循环分解水制氢主要涉及下列反应:
Ⅰ SO2+2H2O+I2===H2SO4+2HI
Ⅱ 2HI![]() H2+I2
H2+I2
Ⅲ 2H2SO4===2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是____________。
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。

0~2 min内的平均反应速率v(HI)=____________。该温度下,H2(g)+I2(g)![]() 2HI(g)的平衡常数K=____________。
2HI(g)的平衡常数K=____________。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡____________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的____________,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。
已知2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1
某氢氧燃料电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是()
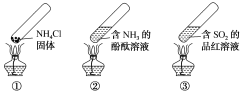
A.加热时,①中上部汇集了NH4Cl固体
B.加热时,②中溶液变红,冷却后又都变为无色
C.加热时,③中溶液变红,冷却后红色褪去,体现SO2的氧化性
D.三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为__________,C的元素符号为____________;B的外围电子的轨道表示式为___________。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________________,其基态原子的电子排布式为________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子的电子排布式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 是中学化学中常见的三种物质,下表各组物质之间通过一步反应不能实现右图所示转化关系的是
X | Y | Z | 箭头上所标数字的反应条件 | ||
A. | NO | NO2 | HNO3 | ①常温遇氧气 |
|
B. | Cl2 | NaClO | HClO | ②通入CO2 | |
C. | Na2O2 | NaOH | NaCl | ③加入H2O2 | |
D. | Al2O3 | NaAlO2 | Al(OH)3 | ④加NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。
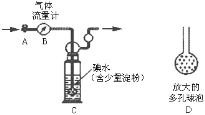
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:_________。
(2)洗气瓶C中的溶液可以酸性高锰酸钾溶液替代,请写出离子方程式:________。
(3)本实验的关键在于关闭气体流量计的时机,应当在什么时候关闭活塞A____________
乙方案:实验步骤如以下流程图所示:
![]()
(4)写出步骤①中反应的化学方程式_________。
(5)如何判断步骤②中沉淀是否完全的方法___________。
(6)经测定当通过的尾气体积为67.2L(已换算成标准状况)时,最终得到固体质量为4.66g,则该尾气中二氧化硫含量(体积分数)为__________(保留到0.01%)
丙方案:将乙中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案________(填是或否)合理,说明理由:___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】轴烯(Radialene)是一类独特的环状烯烃,其环上每一个碳原子都接有一个双键,含n元环的轴烯可以表示为[ n]轴烯,如下图是三种简单的轴烯。下列有关说法不正确的是
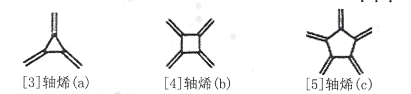
A.a分子中所有原子都在同一个平面上B.b能使酸性KMnO4溶液褪色
C.c与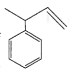 互为同分异构体D.轴烯的通式可表示为C2nH2n(n≥3)
互为同分异构体D.轴烯的通式可表示为C2nH2n(n≥3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用打磨过的铝片进行如下实验,下列分析不合理的是( )
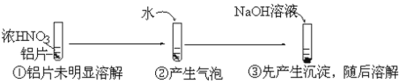
A.①中铝片发生了钝化
B.②中产生的气泡是氮氧化合物,不是氢气
C.③中沉淀溶解的离子方程式是![]()
D.②中加水稀释过程中,仅发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com