
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①根据v=$\frac{△c}{△t}$计算v(C),利用速率之比等于其化学计量数之比计算v(A);
②利用速率之比等于其化学计量数之比计算v(B);
③不同物质的速率之比等于化学计量数之比;
④反应到达平衡时,各组分的物质的量不变.
解答 解:①v(C)=$\frac{0.2mol/L}{2s}$=0.1mol/(L.s),速率之比等于其化学计量数之比,则v(A)=v(C)=0.1mol/(L.s),故①正确;
②利用速率之比等于其化学计量数之比,则v(B)=$\frac{1}{2}$v(C)=0.05mol/(L.s),故②错误;
③不同物质的速率之比等于化学计量数之比,平衡时B与A、C的速率不相等,A、C速率相等,故③错误;
④反应到达平衡时,各组分的物质的量不变,平衡时A、B、C的物质的量均不再变化,故④正确,
故选:B.
点评 本题考查化学反应速率计算、平衡状态判断等,难度不大,注意利用定义式与速率规律计算反应速率.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 下列有关如图所示装置的叙述中错误的是( )
下列有关如图所示装置的叙述中错误的是( )| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -1648.7 kJ.mo1-1 | B. | -1255.3 kJ.mol-1 | ||
| C. | -861.7 kJ.mol-l | D. | +867.1 kJ.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
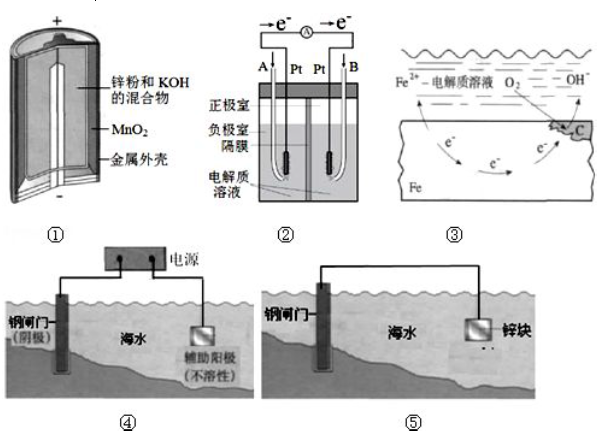
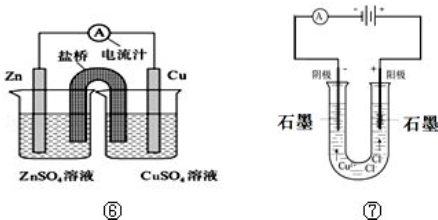
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 离子方程式 |
| A | 向(NH4)2SO4溶液中加入足量Ba(OH)2溶液并加热 | 生成使湿润的红色石蕊试纸变蓝的气体 | NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
| B | 加热滴有酚酞的Na2CO3溶液 | 溶液红色加深 | CO32-+2H2O═H2CO3+2OH- |
| C | 用惰性电极电解氯化镁溶液 | 有白色沉淀和无色无味气体生成 | 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
| D | 向Na2S2O3溶液中加入稀硫酸 | 溶液出现浑浊,生成无色刺激性气味气体 | 2H++S2O32-═S↓+SO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2SO2(g)+O2?2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量 | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(1)△H=-57.3kJ•mol-1,则任何酸碱中和的反应热均为57.3kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2;则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取0.5L溶液,Na+的浓度是0.5mol/L | |
| B. | 取0.1L溶液稀释至l L,SO42-离子浓度是0.05 mol/L | |
| C. | 溶质的离子总数是6.02×1023个 | |
| D. | 该溶液是把0.5molNa2SO4溶于1L水中配制而成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由2Al+6H+=2Al3++3H2↑可知2Fe+6H+═2Fe3++3H2↑ | |
| B. | 由Na与水反应可知2Al+6H2O═2Al(0H)3+3H2↑ | |
| C. | 由Na2O为碱性氧化物,Al2O3为两性氧化物可知,Fe2O3为酸性氧化物 | |
| D. | 由Na不能从CuSO4溶液置换出Cu可知,K也不能与FeCl3溶液反应置换出Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com