
| A.改用0.1mol/L的稀盐酸 | B.加入催化剂 |
| C.改用4mol/L的稀盐酸 | D.加热 |
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:不详 题型:单选题
| A.加入少量的CuSO4溶液 |
| B.将2mol/L的稀硫酸改成98%的浓硫酸 |
| C.将镁粉改为镁条 |
| D.加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将铜与稀硝酸反应的试管浸入热水 |
| B.夏天将牛奶放入冰箱冷藏防止变质 |
| C.将石灰石研碎后与稀盐酸反应制取二氧化碳 |
D.增大2A(g)+B(g)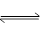 3C(g)+4D(g)体系中A的浓度 3C(g)+4D(g)体系中A的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,n(NO)随时间的变化如下表:
,n(NO)随时间的变化如下表:| 时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4C(g)+5D(g)在2L的密闭容器中进行,1min后A气体减少了0.12mol,则平均每秒中浓度变化正确的是
4C(g)+5D(g)在2L的密闭容器中进行,1min后A气体减少了0.12mol,则平均每秒中浓度变化正确的是| A.A气体:0.05mol·L-1·min-1 | B. B气体:0.075mol·L-1·min-1 |
| C.C气体:0.04mol·L-1·min-1 | D.D气体:0.075mol·L-1·min-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com