
【题目】已知298.15K时,可逆反应:Pb2+(aq)+Sn(s)![]() Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.010mol·L-1,则反应进行的方向是
Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.010mol·L-1,则反应进行的方向是
A. 向右进行 B. 向左进行 C. 处于平衡状态 D. 无法判断
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】已知A为常见烃,是一种水果催熟剂;草莓、香蕉中因为含有F而具有芳香味。现以A为主要原料合成F,其合成路线如下图所示。

(1)A的结构简式为____;D中官能团名称为____。
(2)写出反应①的化学方程式:____________________。
(3)写出反应②的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1871年门捷列夫最早预言了类硅元素锗,锗元素在元素周期表中与硅元素同族,并位于硅的下一周期。1886年德国化学家温克勒发现和分离了锗元素,并以其祖国的名字命名为“Ge”。锗是重要的的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。
已知:①丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀:
②GeCl4易水解,在浓盐酸中溶解度低。
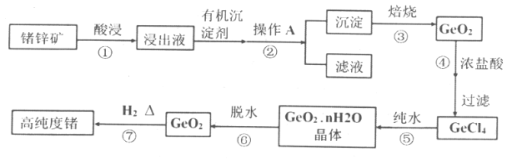
(1)锗元素的原子序数为:___________;锗元素在元素周期表中的位置是:_____________。
(2)GeCl4的结构与SiCl4相似,写出GeCl4的电子式:_______________。
(3)简述步骤①中提高酸浸效率的措施____________、_____________(写两种)。
(4)步骤②操作A是___________(填操作名称)。
(5)步骤③中的物质在___________(填仪器名称)中加热。
(6)步骤④不选用稀盐酸,而选用浓盐酸的原因可能是__________、________(写出两点)。
(7)写出步骤⑤的化学方程式________________。
写出步骤⑦的化学方程式________________。
(8)请写出一种证明步骤⑦反应完全的操作方法__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应:3A(g)+B(g)=2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为:
①v(A)=0.6 mol· L-1·min-1 ②v(B)=0.45 mol· L-1·min-1
③v(C)=0.015 mol· L-1·min-1 ④v(D)=0.45 mol· L-1·min-1
则此反应在不同条件下进行最快的是
A.③B.①C.②D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D 均为短周期元素组成的物质,它们之间符合如下转化关系:
![]()
(1)若A 为可使湿润的红色石蕊试纸变蓝的气态氢化物,X 为水,D 为重要的化工原料。
① A 的电子式为_________________,A→B 的化学方程式为______________________。
②A 和 D 发生化合反应得到的化合物 E 的化学式是___________,用离子方程式表示检验E中阳离子的方法________________。
③写出D的稀溶液与Cu反应的离子方程式____________________________。
(2)若A为非金属单质,X为水,该转化关系为工业生产D的一系列反应。
①将B通入溴水中颜色褪去,体现了B的___________________性,写出该变化的化学方程式________________________。
②A和H2发生化合反应得到的E,在B与E的反应中,氧化产物和还原产物的质量比为_______________________________。
③写出D的浓溶液与Cu反应的化学方程式_________________________________________________________。
(3)若A为烃的含氧衍生物,医疗上常用75%(体积分数)A的水溶液作消毒剂,X为甲醇(CH3OH)。
①A→B的化学方程式为____________________________;C→D的化学方程式为_____________________________________。
②下列说法正确的是___________________________________(选填序号字母)
a. A 可通过葡萄糖分解反应得到 b. B 的官能团的结构简式为-COH
c. C 可与 NaHCO3 反应产生 CO2 d. A 与X 互为同系物
③已知:CH≡CH 在一定条件下可与C反应得到E(结构简式为 CH2=CHOOCCH3),则上述反应的反应类型为_______________________,E中的官能团名称为_____________,E发生加聚反应的化学方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、Q、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。
(1)基态G原子的价电子排布式为____________。
(2)Z、Q、Y三种元素的第一电离能从大到小的顺序为____________(用元素符号表示)。
(3)用电子式表示X2Q的形成过程________________________________________________。
(4)根据等电子体原理,写出YQ的结构式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,金属—空气电池的研究和应用取得很大进步,这种新型燃料电池具有比能量高、污染小、应用场合多等多方面优点。铝—空气电池工作原理如图所示。关于金属—空气电池的说法不正确的是( )

A.铝—空气电池(如上图)中,铝作负极,电子通过外电路到正极
B.为帮助电子与空气中的氧气反应,可使用活性炭作正极材料
C.碱性溶液中,负极反应为Al(s)+3OH-(aq)=Al(OH)3(s)+3e-,每消耗2.7 g Al(s),需耗氧6.72 L(标准状况)
D.金属—空气电池的可持续应用要求是一方面在工作状态下要有足够的氧气供应,另一方面在非工作状态下能够密封防止金属自腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,在4L密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:

(1)t1时刻N的转化率为____________。
(2)0~t3时间内用M表示的化学反应速率为____________mol/(L·min)。
(3)平衡时容器内气体的压强与起始时容器内压强的比值为____________。
(4)该反应的化学方程式为____________;比较t2时刻,正逆反应速率大小:v正____v逆(填“>”、“=”或“<”)。
(5)其他条件不变时,采取下列措施,反应速率的变化情况如何?保持恒温、恒容:①充入少量氦气:____________(填“增大”、“减小”或“不变”,下同);
②充入一定量的气体N:____________。
(6)下列能表示上述反应达到化学平衡状态的是____________。(填编号)
A.v逆(M)=2v正(N) B.M与N的物质的量之比保持不变
C.混合气体密度保持不变 D.容器中压强保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为![]() 溶液,反应为
溶液,反应为![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.充电时,电解质溶液中![]() 向阳极移动
向阳极移动
B.充电时,电解质溶液中![]() 逐渐减小
逐渐减小
C.放电时,负极反应为:![]()
D.放电时,电路中通过![]() 电子,消耗氧气
电子,消耗氧气![]() (标准状况)
(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com