
分析 (1)根据转移电子守恒计算消耗Zn的质量;
(2)Zn和稀盐酸反应生成氢气,如果盐酸恰好完全反应时需要的盐酸体积最少,根据H原子守恒计算消耗n(HCl),再结合V=$\frac{n}{c}$计算盐酸体积;
(3)盐酸物质的量浓度=$\frac{1{0}^{3}ρω}{M}$,再结合V=$\frac{n}{c}$计算盐酸体积.
解答 解:(1)根据转移电子守恒得消耗m(Zn)=$\frac{\frac{4.48L}{22.4L/mol}×2}{2}×65g/mol$=13g,答:消耗锌的质量是13g;
(2)Zn和稀盐酸反应生成氢气,如果盐酸恰好完全反应时需要的盐酸体积最少,根据H原子守恒计算消耗n(HCl)=2n(H2)=2×$\frac{4.48L}{22.4L/mol}$=0.4mol,V=$\frac{n}{c}$=$\frac{0.4mol}{2.0mol/L}$=200mL,
答:至少需要该盐酸体积为200mL;
(3)盐酸物质的量浓度=$\frac{1{0}^{3}ρω}{M}$=$\frac{1000×1.043×7%}{36.5}$=2mol/L,V=$\frac{n}{c}$=$\frac{0.4mol}{2.0mol/L}$=200mL,
答:至少需要该盐酸体积为200mL.
点评 本题考查化学方程式的有关计算,为高频考点,明确各个物理量之间的关系式是解本题关键,注意守恒方法的应用,知道密度、质量分数与物质的量浓度的关系,为易错点.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用高锰酸钾酸性溶液可直接除去乙烷中的乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①=②=③=④ | B. | ①=③>②=④ | C. | ④=②>③=① | D. | ①>③>②>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点.如图是某同学用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计).下列有关判断不正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点.如图是某同学用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计).下列有关判断不正确的是( )| A. | 曲线①代表0.1mol/LKOH溶液滴定CH3COOH溶液的滴定曲线,曲线②代表0.1mol/LKOH溶液滴定HCl溶液的滴定曲线 | |
| B. | 在相同温度下,C点水电离的c(H+)大于A点水电离的c(H+) | |
| C. | 在A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.05 mol/L | |
| D. | 在B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
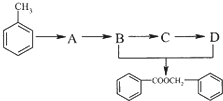
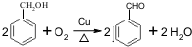 .
. 的化学方程式为
的化学方程式为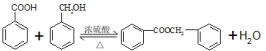 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氧化钠与盐酸:O2-+2H+═H2O | |
| C. | 碳酸氢钠溶液与稀硫酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 烧碱溶液与碳酸氢钠溶液:HCO3-+OH-═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
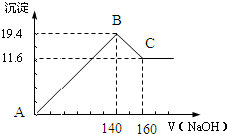
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com