

 ���÷��ӵĺ˴Ź���������2�ַ壮
���÷��ӵĺ˴Ź���������2�ַ壮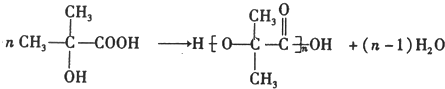 ��F��G�ķ�Ӧ����CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O��
��F��G�ķ�Ӧ����CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O������ A����Է�������Ϊ92.5�ı���һ�ȴ����������к���1��Clԭ�ӣ�ʣ������ʽ��Ϊ92.5-35.5=57���������෨$\frac{57}{12}$=4��9��������Ϊ-C4H9��A�ķ���ʽΪC4H9Cl�������к�������������AΪC��CH3��3Cl��A���������ƴ���Һ�з�����ȥ��Ӧ�õ�BΪ��CH3��2C=CH2��B�����Ӿ۷�Ӧת��Ϊ�߷��ӻ�����CΪ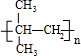 ����CH3��2C=CH2���巢���ӳɷ�Ӧ����DΪ��CH3��2CBr-CH2Br��D�ڼ���������ˮ��ת��ΪEΪ��CH3��2C��OH��-CH2OH��E����������Ӧ����FΪ��CH3��2C��OH��-CHO��F��������õ�G����GΪ��CH3��2C��OH��-COOH���ݴ˽��
����CH3��2C=CH2���巢���ӳɷ�Ӧ����DΪ��CH3��2CBr-CH2Br��D�ڼ���������ˮ��ת��ΪEΪ��CH3��2C��OH��-CH2OH��E����������Ӧ����FΪ��CH3��2C��OH��-CHO��F��������õ�G����GΪ��CH3��2C��OH��-COOH���ݴ˽��
��� �⣺A����Է�������Ϊ92.5�ı���һ�ȴ����������к���1��Clԭ�ӣ�ʣ������ʽ��Ϊ92.5-35.5=57���������෨$\frac{57}{12}$=4��9��������Ϊ-C4H9��A�ķ���ʽΪC4H9Cl�������к�������������AΪC��CH3��3Cl��A���������ƴ���Һ�з�����ȥ��Ӧ�õ�BΪ��CH3��2C=CH2��B�����Ӿ۷�Ӧת��Ϊ�߷��ӻ�����CΪ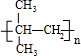 ����CH3��2C=CH2���巢���ӳɷ�Ӧ����DΪ��CH3��2CBr-CH2Br��D�ڼ���������ˮ��ת��ΪEΪ��CH3��2C��OH��-CH2OH��E����������Ӧ����FΪ��CH3��2C��OH��-CHO��F��������õ�G����GΪ��CH3��2C��OH��-COOH��
����CH3��2C=CH2���巢���ӳɷ�Ӧ����DΪ��CH3��2CBr-CH2Br��D�ڼ���������ˮ��ת��ΪEΪ��CH3��2C��OH��-CH2OH��E����������Ӧ����FΪ��CH3��2C��OH��-CHO��F��������õ�G����GΪ��CH3��2C��OH��-COOH��
��1����������ķ�����֪��A�ķ���ʽΪC4H9Cl��FΪ��CH3��2C��OH��-CHO��F�й����ŵ�����Ϊȩ�����ǻ���
�ʴ�Ϊ��C4H9Cl��ȩ�����ǻ���
��2��EΪ��CH3��2C��OH��-CH2OH����Ũ������������£�����������Ԫ��״�������ṹ��ʽΪ  ���÷��ӵĺ˴Ź���������2�ַ壬
���÷��ӵĺ˴Ź���������2�ַ壬
�ʴ�Ϊ����CH3��2C��OH��-CH2OH�� ��2��
��2��
��3��GΪ��CH3��2C��OH��-COOH��G��һ�����������ɸ߷��ӻ������Ӧ�Ļ�ѧ����ʽΪ��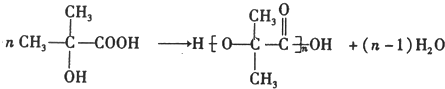 ��F��G�ķ�Ӧ�Ļ�ѧ����ʽΪ��CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O��
��F��G�ķ�Ӧ�Ļ�ѧ����ʽΪ��CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O��
�ʴ�Ϊ��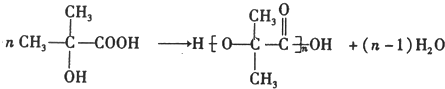 ����CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O��
����CH3��2C��OH��-CHO+2Cu��OH��2$\stackrel{��}{��}$��CH3��2C��OH��-COOH+Cu2O��+2H2O��
��4��GΪ��CH3��2C��OH��-COOH��G��ͬ���칹�������࣬�ܷ���������Ӧ��Ϊ����������������Ʒ�Ӧ�ų����壬������-OH������������ͬ���칹���У�HOCH2CH2CH2OOCH��CH3CH��OH��CH2OOCH��CH3CH2CH��OH��OOCH��HCOOC��CH3��CH2OH��HCOOC��OH����CH3��2�������֣�
�ʴ�Ϊ��5��
���� ���⿼���л�����ƶϣ��Ƕ��л���ѧ֪ʶ���ۺϿ��飬�ƶ�A�Ľṹ�ǽ���Ĺؼ����ܽϺõĿ���ѧ���ķ�����˼ά�������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���¶Ȳ��䣬�����������һ������ʱA��Ũ����ԭ����0.48������a+b����d | |
| B�� | ��������Ӧ��ʼƽ��ʱA��B��ת������ȣ���A��B�����ʵ���֮��Ϊa��b | |
| C�� | ��ƽ����ϵ������M mol���ٳ���bmolB���ﵽƽ��������Ϊ��M+b��mol����a+b=c+d | |
| D�� | ��a+b=d�����������¶�����ʱ��ƽ�������ƶ��������������ѹǿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
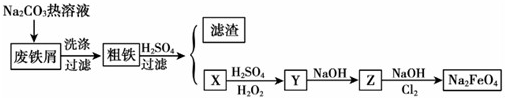
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ͼ�����еķ�Ӧ��Ϊ������ԭ��Ӧ | |
| B�� | ��Ӧ�٢ھ�Ϊ���ӷ�Ӧ | |
| C�� | ��Ӧ�ڢ۶��ܲ����������Ҳ���������������Al��������ת�Ƶ������ֱ���� | |
| D�� | ��Ӧ�٢ڢ�����������ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ҫԭ�ϣ�̼��� ʳ�÷�����ÿ��һ�Σ�ÿ��һƬ����ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺
���ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com