
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
A.原混合物中铜和铁各0.15 mol B.稀硝酸的物质的量浓度为1 mol·L-1
C.第一次剩余9.6 g金属为铜和铁 D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO
A
【解析】
试题分析:向反应后的溶液中加入KSCN溶液,溶液不变红,说明在溶液中存在的离子是Fe2+;溶液中存在Fe2+、Cu2+。两次加入的酸相同,产生的NO的物质的量相同,则转移的电子的物质的量也相同。每一次反应产生NO的物质的量为2.24L÷22.4L/mol=0.1mol,电子转移为0.1mol×3=0.3mol.由于金属活动性Fe>Cu,所以首先溶解的是金属Fe,根据反应方程式是3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O。可知消耗的金属Fed的物质的量为3/2×0.1mol=0.15 mol.若剩余的金属都是Cu,则n(Cu)= 9.6 g÷64g/mol=0.15 mol;由于Cu是+2价金属,所以电子转移数目为0.15 mol×2=0.3mol。正好与题干吻合。因此原混合物中铜和铁各0.15 mol。每一次加入硝酸的物质的量为8/2×0.1mol=0.4mol.因此硝酸的物质的量浓度为0.4mol÷0.2L=2mol/L.若再加入上述200 mL稀硝酸,会发生反应:NO3-+4H++3Fe2+= 3Fe3++NO↑+2H2O,n(Fe2+)=0.15 mol;反应需要消耗H+的物质的量为0.15 mol ×4/3=0.2mol;实际加入的n(H+)=0.4mol,多于需要量,因此放出的气体按照Fe2+来计算。根据离子方程式可知可还会产生NO的的物质的量为0.05 mol。在标准状况下体积为1.12L。因此正确选项为A。
考点:考查铜和铁的混合物与硝酸发生反应的情况的知识。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源:2013-2014陕西省岐山县第二学期高二期末化学试卷(解析版) 题型:填空题
(10分)充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍。
(1)求该有机物的分子式。
(2)该有机物链状同分异构体的结构简式为: 。
(3) 若有机物A在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省岐山县第二学期高一期末化学试卷(解析版) 题型:选择题
下列化学用语表示正确的是
A.N2的电子式:N : N B.乙酸的分子式:CH3COOH
C.硫离子结构示意图: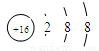 D.乙烷的结构式:CH3CH3
D.乙烷的结构式:CH3CH3
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省富平县高二下学期期末考试化学试卷(解析版) 题型:选择题
A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B最简式一定相同 B.A和B不可能是同系物
C.A和B一定是同分异构体D.A和B的化学性质相似
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:填空题
(10分)下图是研究铜与浓硫酸的反应装置:
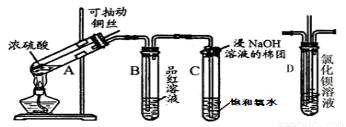
(1)A试管中发生反应的化学方程式为 。
(2)反应一段时间后,可观察到B试管中的现象为 。
(3)C试管口浸有NaOH溶液的棉团作用是 。
(4)实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是 。
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1 |
附表铜与浓硫酸反应产生黑色物质的相关性质 |
资料2 | X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。 |
仅由上述资料可得出的正确结论是 。
A.铜与浓硫酸反应时所涉及的反应可能不止一个 B.硫酸浓度选择适当,可避免最后产物中出现黑色物质;C.该反应发生的条件之一是硫酸浓度≥15 mol·L D.硫酸浓度越大,黑色物质越快出现、越难消失
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:选择题
mA(g)+nB(g)  pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:选择题
一定温度下,对于反应N2+O2 2NO在密闭容器中进行,下列措施能增大反应速率的是 ( )。
2NO在密闭容器中进行,下列措施能增大反应速率的是 ( )。
A.降低温度 B.恒容充入氮气 C.恒压充入氦气 D.恒容充入氦气
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:填空题
(14分)有A、B、C、D、F、G六种短周期主族元素,它们的原子序数依次增大。B元素的最高正价与最低负价的绝对值相等,D元素原子最外层电子数是次外层电子数的3倍,F元素在地壳中含量居第二位;A与B、C、D分别构成电子数相等的分子Q、X、Y;化合物AG在空气中与X反应产生白烟Z。
请回答下列问题:
G的原子结构示意图为 ,A2D2电子式为 ,
BD2的结构式为 ,Q的分子空间结构为 。
(2)固体Z为 晶体(填晶体类型),Z中所含化学键类型有 。
(3)在D同主族元素氢化物中,Y的沸点反常,原因是 。
(4)B、F、G元素非金属性由强到弱的顺序为 ,若用下图装置验证这三种元素非金属性强弱,则在装置中加入的试剂分别为:Ⅰ ,Ⅱ ,Ⅲ 。(填化学式)
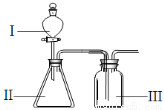
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市名校联盟高三三诊理综化学试卷(解析版) 题型:选择题
化学学习中,推理是一种重要的学习方法,下列推论正确的是
A.由“BF3和SO3互为等电子体”,可推知二者均为非极性分子
B.由“同主族元素性质相似,CO2为直线形分子”,可推知SiO2为直线形分子
C.由“SiH4的熔沸点比CH4高”,可推知PH3的熔沸点比NH3高
D.由“C、N、O三种元素的电负性C<N<O”,可推知第一电离能C<N<O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com