
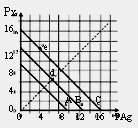
|
| A��A����AgCl��C����AgI | B��e���ʾ�ɹ�����KI��AgNO3��Ӧ����AgI���� |
| C��d������ˮ�м���������AgBr�γɵı�����Һ | |
| D��B��һ����AgBr |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊ����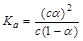 �����������������ƹ��壬��CH3COOH �����������������ƹ��壬��CH3COOH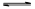 CH3COO����H�������ƶ�������С��Ka��С CH3COO����H�������ƶ�������С��Ka��С |
B�������£���Ӧ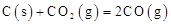 �����Է����У���÷�Ӧ�� �����Է����У���÷�Ӧ��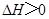 |
C��һ���¶��£��Ȼ��ˮ�����ӷ���ʽ��NH+4+H2O NH3��H2O+H+������KW��ʾ�����ӻ��� NH3��H2O+H+������KW��ʾ�����ӻ���Kb��ʾ��ˮ���볣�������Ȼ��ˮ��ƽ�ⳣ��K=KW/Kb |
| D��һ�֡��˹��̵������·������ڹ��������£�N2�ݴ���������ˮ����������Ӧ����NH3������,��֪�� |

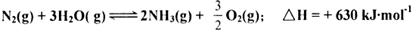
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ڷ��Ⱥ������ӵķ�Ӧ�������Է����� |
| B����Һ��ϡ�����У���Һ�е�����������Ũ�ȶ���С |
| C����ij���淴Ӧ���ԣ���ƽ�ⳣ��KֵԽ��Ӧ���ת����ҲԽ�� |
| D����2.0 mLŨ�Ⱦ�Ϊ0.1 mol/L��KCl��KI�����Һ�еμ�1~2��0.01 mol/L AgNO3��Һ���������ʻ�ɫ��˵��AgCl��Ksp��AgI��Ksp�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ˮ��ԭ����Al3+ˮ�����Al(OH)3���壬Al(OH)3����������ˮ�е��������ʣ���ʹ֮���� |
| B��Ħ���ε��Ʊ�ԭ��Ϊ��6H2O+FeSO4+(NH4)2SO4=(NH4)2Fe(SO4)?6H2O����Ӧ֮�����ܽ��е�ԭ����(NH4)2Fe(SO4)?6H2O�ܽ����С |
| C����п��Ƥ�������ܽ⣬���Ʋ㷴Ӧ��ȫʱ���������������ʻ�ͻȻ���� |
| D�������ͷֱ�ӽ���Ʒ����Һ�У����Լ�����ͷ���Ƿ�����Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
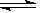 N2O4��g������H��0����һ�������£���Ӧ�ﵽƽ��ı������������ٴδﵽƽ���������������ɫ������ǣ� ��
N2O4��g������H��0����һ�������£���Ӧ�ﵽƽ��ı������������ٴδﵽƽ���������������ɫ������ǣ� ��| A���٢ڢۢ� | B���٢ڢ� | C���٢� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ˮ�м��ᣬNH4+ ��Ũ������ |
| B���ϳɰ���ҵ�в��ϴӷ�Ӧ�������Һ����������� |
| C��ʵ�����г����ű���ʳ��ˮ�ķ����ռ�Cl2 |
| D���ϳɰ�������500�����ҵ��¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
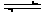 2C(g)��2S���÷�Ӧ��������V (A2)��0.4mol��(L��s)��V (B2)="1.2" mol��(L��s) ��V (C)= 0.8mol��(L��s) ���x��y��ֵ�ֱ�Ϊ
2C(g)��2S���÷�Ӧ��������V (A2)��0.4mol��(L��s)��V (B2)="1.2" mol��(L��s) ��V (C)= 0.8mol��(L��s) ���x��y��ֵ�ֱ�Ϊ�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com