
| A. | 18y/x | B. | 9y/x | C. | 18y/x mol-1 | D. | 9y/x mol-1 |
科目:高中化学 来源: 题型:解答题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;由A→B的反应类型是:还原反应.
;由A→B的反应类型是:还原反应. .
. 为原料制备化合物X(
为原料制备化合物X( )(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
)(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 阳离子 | Fe3+、Al3+、Fe2+、Ba2+、Na+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.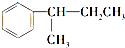 $\stackrel{酸性KMnO_{4}溶液}{→}$
$\stackrel{酸性KMnO_{4}溶液}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质经测定,只含有一种组成元素,则该物质一定是单质 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物 | |
| D. | 纯净的硫酸是纯净物,而纯净的盐酸是混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com