
| 欲除去的少量杂质 | 方法 | 反应的离子方程式 |
| (1)Na2CO3溶液中的NaHCO3 | ||
| (2)NaCl溶液中的Na2CO3 | ||
| (3)NaHCO3溶液中的Na2CO3 |
分析 (1)NaHCO3可与NaOH反应生成Na2CO3;
(2)可加入盐酸除杂;
(3)Na2CO3溶液和二氧化碳反应生成NaHCO3.
解答 解:(1)NaHCO3可与NaOH反应生成Na2CO3,反应的离子方程式为HCO3-+OH-═CO32-+H2O,故答案为:向溶液中滴加适量的氢氧化钠; HCO3-+OH-═CO32-+H2O;
(2)盐酸和碳酸钠反应生成氯化钠、二氧化碳和水,可加入盐酸除杂,反应的离子方程式为CO32-+2H+═CO2↑+H2O,
故答案为:加入适量的盐酸至无气体放出;CO32-+2H+═CO2↑+H2O;
(3)Na2CO3溶液和二氧化碳反应生成NaHCO3,反应的离子方程式为CO32-+CO2+H2O═2HCO3-,故答案为:通入过量的二氧化碳气体; CO32-+CO2+H2O═2HCO3-.
点评 本题考查物质的分离、提纯和除杂等问题,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离,注意把握离子方程式的书写.


科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | 3NO2+H2O=2HNO3+NO | ||
| C. | 2Al+2NaOH+6H2O=2NaAlO2+3H2↑ | D. | CaCO3=CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
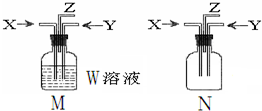 利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )
利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )| 选项 | 所用装置 | 描述 | 结论 |
| A | M | W:BaCl2;X:CO2 Y:SO2 | M中有白色沉淀生成 |
| B | M | W:饱和食盐水;先通入X:CO2,再通入Y:NH3 | M中制得小苏打 |
| C | N | X:NH3 Y:Cl2 | Z出口有白烟产生 |
| D | N | X:NH3Y:O2 | Z出口有红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液的pH<7 | |
| B. | 某物质的溶液中由水电离出的c(H+)=1×10-amol•L-1,若a>7,则该溶液的pH一定为14-a | |
| C. | 将0.2mol•L-1的某一元酸HA溶液和0.1mol•L-1 NaOH溶液等体积混合后,混合溶液的pH大于7,则反应后的混合溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-) | |
| D. | pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH=7,则反应后的混合溶液中:2c(R2-)+c(HR-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤③①⑥ | B. | ③②④①⑤⑥ | C. | ③④②⑤①⑥ | D. | ②④③⑤①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 点燃的镁条在二氧化碳中继续燃烧 | B. | Ca(OH)2与NH4Cl的反应 | ||
| C. | 灼热的碳与二氧化碳的反应 | D. | 酸碱中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比 |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com