
 .
. .
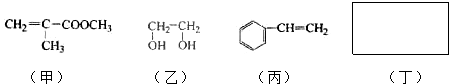
. 分析 (1)甲含有碳碳双键和酯基等官能团;
(2)一种不含甲基的链状羧酸为CH2=CH-CH2-CH2-COOH;
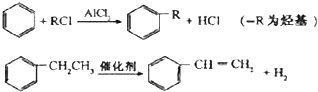
(3)由乙醇$\stackrel{一定条件}{→}$A$\stackrel{Br_{2}/CCl_{4}}{→}$B$\stackrel{氢氧化钠溶液}{→}$乙可知,乙醇发生消去反应生成A为乙烯、乙烯加成生成B为1,2-二溴乙烷,B水解生成C为乙二醇;
(4)发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、
、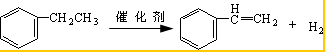 ;
;
(5)丁与FeCl3溶液作用显现特征颜色,且丁的核磁共振氢谱图象仅有2个波峰,强度比为2:1,说明分子中含有酚羟基,分子结构对称.
解答 解:(1)甲含有碳碳双键和酯基等官能团,不含氧的官能团为碳碳双键,含双键、与溴水、高锰酸钾反应褪色,故答案为:碳碳双键;ac;
(2)甲的同分异构体中不含甲基的链状羧酸为CH2=CH-CH2-CH2-COOH,故答案为:CH2=CH-CH2-CH2-COOH;
(3)由乙醇$\stackrel{一定条件}{→}$A$\stackrel{Br_{2}/CCl_{4}}{→}$B$\stackrel{氢氧化钠溶液}{→}$乙可知,乙醇发生消去反应生成A为CH2=CH2,乙烯加成生成B为1,2-二溴乙烷,B水解生成C为乙二醇,则B→乙的化学方程式为BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr,故答案为:CH2=CH2;BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr;
(4)发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、发生反应分别为CH2=CH2+HCl→CH3CH2Cl、
、发生反应分别为CH2=CH2+HCl→CH3CH2Cl、 、
、 ,
,
其中属于取代反应的为 ,故答案为:
,故答案为: ;
;
(5)丁与FeCl3溶液作用显现特征颜色,且丁的核磁共振氢谱图象仅有2个波峰,强度比为2:1,说明分子中含有酚羟基,分子结构对称,应为 ,相对分子质量为110,
,相对分子质量为110,
故答案为: .
.
点评 本题考查有机物的合成与推断,侧重于有机物官能团的性质的考查,为高考常见题型,难度不大,注意把握有机物官能团的性质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 ;A→F
;A→F .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 周期表中第VA族元素的最高价氧化物对应水化物的化学式均为H3RO4 | |
| B. | O${\;}_{2}^{2-}$与S2-具有相同的质子数和电子数 | |
| C. | 氕、氘、氚分别与O原子形成的水H2O、D2O、T2O的化性质不同 | |
| D. | 形成离子键的阴阳离子间只存在静电吸引力 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | (3)(4)(2)(1) | B. | (3)(1)(4)(2) | C. | (4)(3)(1)(2) | D. | (3)(4)(1)(2) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液使酚酞试液变红:S2-+2H2O?2OH-+H2S | |
| B. | 用右图装置电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | NaHCO3溶液使酚酞试液变红:HCO3-+H2O?H3O++CO32- | |
| D. | 用AlCl3溶液使石蕊试液变红:Al3++3H2O?Al(OH)3+3 H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com