
在分别含有下列微粒的各种溶液中, 无论加入少量的浓盐酸或固体烧碱或高锰酸钾晶体都能使微粒的浓度较明显减少, 这种微粒是
[ ]
A. HS-
B. Fe2+
C. HCO3-
科目:高中化学 来源: 题型:
(8分)研究物质的结构是研究物质性质的的基础,分析下列微粒的结构,完成问题:
(1) 根据VSEPR理论,BCl3的立体结构为:_______________,HCN的立体结构为:_________________。(文字表述,不必画图)两分子中中心原子的杂化类型分别为_________ ___________ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为 ,
的未成对电子数是 。
(3)中的
与
互为等电子体。已知
、
两种粒子中各原子最外层均为8电子稳定结构。
的电子式可表示为 ;
中含有的
键数目为 。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年山东省莘县一中高二下学期第一次月考化学试卷 题型:填空题
(8分)研究物质的结构是研究物质性质的的基础,分析下列微粒的结构,完成问题:
(1) 根据VSEPR理论,BCl3的立体结构为:_______________,HCN的立体结构为:_________________。(文字表述,不必画图)两分子中中心原子的杂化类型分别为_________ ___________ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为 , 的未成对电子数是 。
的未成对电子数是 。
(3)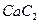 中的
中的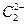 与
与 互为等电子体。已知
互为等电子体。已知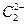 、
、 两种粒子中各原子最外层均为8电子稳定结构。
两种粒子中各原子最外层均为8电子稳定结构。 的电子式可表示为 ;
的电子式可表示为 ; 中含有的
中含有的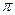 键数目为 。
键数目为 。
查看答案和解析>>
科目:高中化学 来源:2012届山东省高二下学期第一次月考化学试卷 题型:填空题
(8分)研究物质的结构是研究物质性质的的基础,分析下列微粒的结构,完成问题:
(1) 根据VSEPR理论,BCl3的立体结构为:_______________,HCN的立体结构为:_________________。(文字表述,不必画图)两分子中中心原子的杂化类型分别为_________ ___________ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为 ,
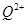 的未成对电子数是 。
的未成对电子数是 。
(3)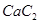 中的
中的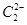 与
与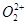 互为等电子体。已知
互为等电子体。已知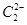 、
、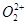 两种粒子中各原子最外层均为8电子稳定结构。
两种粒子中各原子最外层均为8电子稳定结构。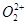 的电子式可表示为 ;
的电子式可表示为 ;
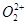 中含有的
中含有的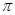 键数目为
。
键数目为
。
查看答案和解析>>
科目:高中化学 来源:???????????2011?????????ε??п??? 题型:填空题
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.诺贝尔物理学奖曾授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型为 ,同层分子间的主要作用为 。
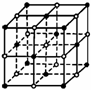 (2)K3[Fe(CN)6]晶体中含有的化学键类型为 ,
(2)K3[Fe(CN)6]晶体中含有的化学键类型为 ,
Fe3+与CN-之间能够形成化学键的原因是 。
(3)等物质的量的氧化物MO与SiC的电子总数相等,则M2+
离子的核外电子排布式为 。
MO是优良的耐高温材料,其晶体结构与NaCl晶体相
似,晶体中与每个M2+等距离且最近的几个O2-所围成
的空间几何构型为 。
MO的熔点比CaO的高,原因是 。
B.某化工废液中可能含有下列微粒:Al3+、Fe3+、NO2-、甘油分子。化学兴趣小组的同学设计了下列实验验证这些微粒的存在。
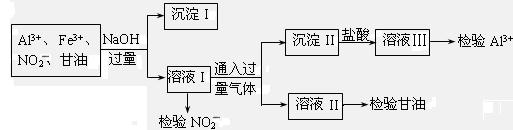
(1)分离出沉淀I的操作名称是 ,利用沉淀I可检验出 离子。
(2)通入的过量气体是 。(写化学式)
(3)用酸性KI溶液检验NO2-离子的离子方程式为 。
(4)写出检验甘油所发生反应的化学方程式: 。
(5)若向溶液III中先加足量NH4F后加氨水来检验Al3+离子,则能否达到目的?
答: (填“能”或“不能”);原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com