
| A. | 先从b管通入NH3再从a管通入CO2 | B. | 先从a管通入CO2再从b管通入NH3 | ||
| C. | 广口瓶内有白色沉淀析出 | D. | c中试剂为碱石灰 |
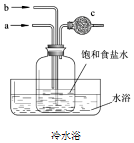
分析 氨气极易溶于水,需要防止倒吸,则a通入NH3、b通CO2;二氧化碳与水反应形成不稳定的碳酸,使水吸收二氧化碳量较少,而把二氧化碳通入溶有氨气而呈碱性的水中,会使生成的碳酸与氨水发生反应,而增大二氧化碳气体的吸收,所以正确操作为:先从a管通入NH3再从b管通入CO2,据此进行解答.
解答 解:A.应该a通入NH3、b通CO2,否则氨气易发生倒吸,故A错误;
B.二氧化碳与水反应形成不稳定的碳酸,使水吸收二氧化碳量较少,而把二氧化碳通入溶有氨气而呈碱性的水中,会使生成的碳酸与氨水发生反应,而增大二氧化碳气体的吸收,应该先通入氨气再通二氧化碳,故B错误;
C.反应的化学方程式为:NH3+CO2+H2O+NaCl═NH4Cl+NaHCO3↓,由于碳酸氢钠的溶解度很小,以晶体形式析出,故C正确;
D.氨气有毒,c的作用是吸收逸出氨气,防止环境污染,碱石灰不能吸收氨气,可用氯化钙,故D错误;
故选C.
点评 本题考查侯氏制碱法的应用,题目难度中等,明确通入气体的导管及先后顺序为解答关键,注意掌握侯氏制碱法原理,试题侧重考查学生的分析、理解能力及化学实验能力.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
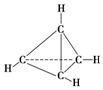 一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )
一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )| A. | 1种 | B. | 2种 | C. | 4种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、
、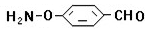 、
、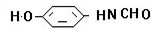 、
、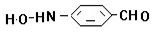 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C与氧元素形成的化合物一定属于碱性氧化物 | |
| B. | 最高价氧化物对应的水化物的酸性:E>D>A | |
| C. | 简单氢化物的沸点:E>B | |
| D. | 原子半径:C>D>E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmolNa2O和Na2O2混合物中含有的阴阳离子总数大于3NA | |
| B. | 常温常压下,20gD2O分子中所含中子数为10NA | |
| C. | 50ml12mol•L-1的盐酸与足量的MnO2共热转移的电子数为0.3 NA | |
| D. | 密闭容器中2mol NO和Imol的O2,充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度℃ | ||
| 浓度/(mol•L-1) | 体积/mL | 浓度/(mol•L-1) | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是( )| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- | |
| B. | A点溶液中的溶质为NaCl、NaHCO3 | |
| C. | 混合物中NaOH的质量0.60 g | |
| D. | 当加入35 mL盐酸时,产生CO2的体积为224 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com