
| A、酸性强弱:HClO4>HBrO4>HIO4 |
| B、氢化物稳定性:HF>H2O>NH3 |
| C、沸点高低:HF>HBr>HCl |
| D、密度大小:K>Na>Li |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、鸡蛋清中加入CuSO4溶液产生盐析 |
| C、乙酸乙酯、油脂与NaOH溶液反应均有乙醇生成 |
| D、石油分馏可得到汽油、煤油等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 实验室制硝基苯 |
B、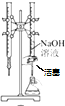 用已知浓度的NaOH溶液测定盐酸浓度的实验 |
C、 在铁制品表面镀锌操作 |
D、 称取一定量的NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇、乙醛、乙酸都能与H2O形成分子间氢键 |
| B、丙烯中最多有7个原子共平面 |
| C、乙醇与金属钠反应比水与金属钠反应更剧烈,羟基H活性更高 |
D、乙酸、甲酸甲酯和羟基乙醛 互为同分异构体 互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com