
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏操作时,冷凝水从下口进、上口出 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |


科目:高中化学 来源: 题型:
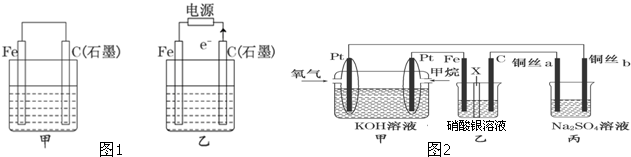
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 s |
| B、2.5 s |
| C、5 s |
| D、10 s |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150ml 1 mol?L-1氯化钠溶液 |
| B、75ml 2 mol?L-1氯化镁溶液 |
| C、50ml 3mol?L-1氯化钾溶液 |
| D、200ml 1.5 mol?L-1氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类物质是绿色植物光合作用的产物 |
| B、淀粉和纤维素都是天然高分子化合物 |
| C、食物中的纤维素对人体没有任何益处 |
| D、维生素、无机盐和水都是人体需要的营养素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤④⑦ | B、①③④⑦ |
| C、②③④⑤⑦ | D、②④⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com