
| 1.56g |
| 78g/mol |
| 1.56g |
| 78g/mol |
| 1.6g |
| 1.56g+20.00g-0.32g |
| 1.6g |
| 1.56g+20.00g-0.32g-xg |
| 53g |
| 153g |


科目:高中化学 来源: 题型:
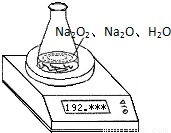
 某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.
某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市杨浦区高三上学期期末学业质量调研化学试卷(解析版) 题型:实验题
亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
已知:室温下,①2NO+Na2O2→2NaNO2 ②3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O;

③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和 ,为避免产生这些副产物应在B、C装置间增加装置E,画出E并注明E中盛放的药品名称 。
(5)写出检验C产物中是否含碳酸钠的方法 。
(6)将1.56g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.
某种含有少量氧化钠的过氧化钠试样质量为1.56g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12g.查看答案和解析>>
科目:高中化学 来源:姜淮培训中心高三化学试题及答案(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com