
| H2O |
| 5.3g |
| 106g/mol |
| 15.4g |
| 44g/mol |
| 2.7g |
| 18g/mol |
| 0.35mol |
| 0.05mol |
| 0.15mol×2 |
| 0.05mol |
| 106-12×7-6 |
| 16 |
| 2×7+2-6 |
| 2 |
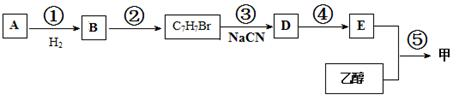
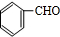 ,苯甲醛和氢气发生加成反应生成B,结合反应②产物的分子式可知,醛基发生加成反应B为
,苯甲醛和氢气发生加成反应生成B,结合反应②产物的分子式可知,醛基发生加成反应B为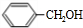 ,B与HBr发生取代反应生成
,B与HBr发生取代反应生成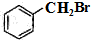 ,
, 和氰化钠反应生成D,结合题给信息知,D的结构简式为:
和氰化钠反应生成D,结合题给信息知,D的结构简式为: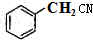 ,
, 反应生成E,E能和乙醇反应生成酯,则E是羧酸,结合题给信息知,E是
反应生成E,E能和乙醇反应生成酯,则E是羧酸,结合题给信息知,E是 ,甲是
,甲是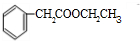 ,据此解答.
,据此解答.| 5.3g |
| 106g/mol |
| 15.4g |
| 44g/mol |
| 2.7g |
| 18g/mol |
| 0.35mol |
| 0.05mol |
| 0.15mol×2 |
| 0.05mol |
| 106-12×7-6 |
| 16 |
| 2×7+2-6 |
| 2 |
 ,苯甲醛和氢气发生加成反应生成B,结合反应②产物的分子式可知,醛基发生加成反应B为
,苯甲醛和氢气发生加成反应生成B,结合反应②产物的分子式可知,醛基发生加成反应B为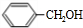 ,B与HBr发生取代反应生成
,B与HBr发生取代反应生成 ,
, 和氰化钠反应生成D,结合题给信息知,D的结构简式为:
和氰化钠反应生成D,结合题给信息知,D的结构简式为: ,
, 反应生成E,E能和乙醇反应生成酯,则E是羧酸,结合题给信息知,E是
反应生成E,E能和乙醇反应生成酯,则E是羧酸,结合题给信息知,E是 ,甲是
,甲是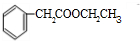 ,
, ,其苯环的一氯代物共有3种,故答案为:C7H6O;3;
,其苯环的一氯代物共有3种,故答案为:C7H6O;3; 中溴原子被-CN取代生成
中溴原子被-CN取代生成 ,属于取代反应,故答案为:取代反应;
,属于取代反应,故答案为:取代反应; ,
, ;
;

科目:高中化学 来源: 题型:
| t(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.50 | 0.35 | 0.28 | 0.25 | 0.25 | 0.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2?Ca2++2OH- |
| B、H2SO3?2H++SO32- |
| C、NaHS?Na++HS- |
| D、HCO3-?H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HO-CH2-CH2-OH |
B、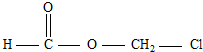 |
C、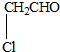 |
D、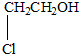 |
查看答案和解析>>
科目:高中化学 来源: 题型:
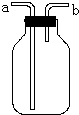 (1)如图的装置在实验室中用途比较广泛:
(1)如图的装置在实验室中用途比较广泛:查看答案和解析>>
科目:高中化学 来源: 题型:
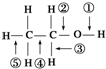 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )| A、和金属钠反应时键①断裂 |
| B、在铜催化共热下与O2反应时断裂①和③ |
| C、在铜催化共热下与O2反应时断裂①和⑤ |
| D、在空气中完全燃烧时断裂①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32.64 g |
| B、65.28 g |
| C、3.84 g |
| D、38.4 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com