
【题目】H2S是二元弱酸,溶液中存在H2S![]() H++HS-、HS-
H++HS-、HS-![]() H++S2-。
H++S2-。
(1)向H2S溶液中加入CuSO4溶液时,电离平衡向_______移动,c(H+)________,c(S2-)________。
(2)向H2S溶液中加入NaOH固体时,电离平衡向_______移动,c(H+)________,c(S2-)________。
(3)若将H2S溶液加热至沸腾,c(H2S)________。
(4)若要增大H2S溶液中的c(S2-),最好加入__________。
【答案】右 增大 减小 右 减小 增大 减小 NaOH固体(合理即可)
【解析】
H2S是二元弱酸,其电离为可逆反应,若加入与其反应的物质,则破坏原来的平衡,导致平衡发生移动。
(1)加入CuSO4溶液时,则Cu2++ S2-=CuS↓不溶于酸,溶液中的c(S2-)减小,平衡向右移动,c(H+)增大,故答案为:右,增大,减小;(2)加入NaOH固体时,H++ OH-=H2O,c(H+)减小,平衡向右移动,c(S2-)增大,故答案为:右,减小,增大;(3)若将H2S溶液加热至沸腾,电离为吸热反应,升高温度平衡向电离的方向移动,同时H2S溶解度减小,气体逸出,c(H2S)减小,答案为减小;(4)若要增大H2S溶液中的c(S2-),使平衡右移,答案为NaOH固体或加热(不考虑气体逸出)。


科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示。下列说法中不正确的是
2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示。下列说法中不正确的是

A. t0~t1时,v(正)>v(逆)
B. I、Ⅱ两过程分别达到平衡时,A的体积分数Ⅰ=Ⅱ
C. t2 时刻改变的条件可能是向密闭容器中加A物质
D. Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ=Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟合成医药中间体X。

请回答:
(1)下列说法正确的是_________。
A.化合物B不能使溴水褪色
B.化合物C能与CuO发生氧化反应
C.化合物D的分子式是C9H10O2Br
D.化合物E到F发生的是加成反应
(2)化合物H的结构简式是________。
(3)已知I→X是取代反应,写出该反应的化学方程式________。
(4)化合物G的同分异构体有以下特征:①含有苯环;②1H﹣NMR谱显示分子中有3种氢原子;③分子结构中不存在氧氧键。请写出所有符合要求的结构简式(或键线式)___。
(5)已知:①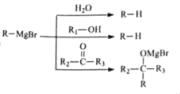 ;②
;② ,请结合题目中已知信息设计由
,请结合题目中已知信息设计由![]() 合成
合成![]() 的路线________________________(用流程图表示)。
的路线________________________(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产生活中用途广泛。回答下列问题:
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是______(填序号)。
A.
B.
C.
D.
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如下图所示的离子。

①该离子中含有化学键的类型有______(填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
②该离子中碳原子的杂化方式有______。
③H、N、Cu三种元素的电负性由大到小的顺序是______。
(3)甲醇(CH3OH)在Cu催化作用下被氧化成甲醛(HCHO)。甲醛分子内σ键与π键个数之比为______。甲醇分子内的O-C-H键角______(填“大于”“等于”或“小于”)甲醛分子内的O-C-H键角。
(4)某磷青铜晶胞结构如下图所示:

①其中原子坐标参数A为(0,0,0);B为(0,![]() ,
,![]() )。则P原子的坐标参数为______。
)。则P原子的坐标参数为______。
②该晶体中距离Cu原子最近的Sn原子有______个,这些Sn原子所呈现的构型为______。
③若晶体密度为agcm3,最近的Cu原子核间距为______pm(用含NA和a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;
④将得到的产物熔融电解得到镁。
下列说法不正确的是( )
A. 此法的优点之一是原料来源丰富B. ①②③步骤的目的是从海水中提取镁盐
C. ①②③步骤涉及化合、分解和复分解反应D. 第①到第④步的反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)若电解食盐水时消耗NaCl的质量为234 g,则在理论上最多可得氯气的体积为________升(标准状况)。
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制100mL 1.0 mol/L Na2CO3溶液,正确的方法是
① 将10.6 g Na2CO3 溶于100mL水中
② 将28.6g Na2CO3·10H2O溶于水配成100 mL溶液
③ 将20 ml 5.0 mol/L Na2CO3溶液加水稀释至100 mL
A. ①②③ B. ②③ C. 只有② D. 只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将如图所示实验装置的K闭合,下列判断正确的是

A. Cu电极上发生还原反应
B. 电子沿Zn→a→b→Cu路径流动
C. 盐桥中K+向移向ZnSO4溶液
D. 片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是典型晶体的结构示意图,从①到⑥对应正确的是:
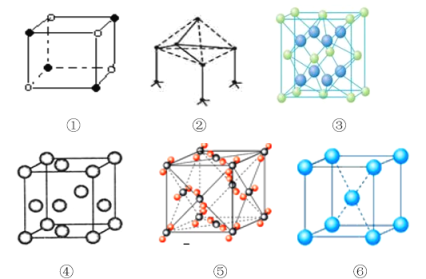
选项 | ① | ② | ③ | ④ | ⑤ | ⑥ |
A | NaCl | 单质硅 | CaF2 | Au | CO2 | K |
B | CaF2 | SiC | 金刚石 | Cu | CO2 | CsCl |
C | CsCl | 金刚石 | CaF2 | Cu | CO2 | Mg |
D | NaCl | BN | Au | CaF2 | CO2 | Na |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com