
| A£® | µČĪļÖŹµÄĮæµÄCH4ŌŚ·“Ó¦¢Ł”¢¢ŚÖŠ×ŖŅʵē×ÓŹżĻąĶ¬ | |
| B£® | ÓÉ·“Ó¦¢ŁæÉĶĘÖŖ£ŗCH4£Øg£©+4NO2£Øg£©ØT4NO£Øg£©+CO2£Øg£©+2H2O£Øl£©”÷H£¾-574 kJ•mol-1£® | |
| C£® | 4NO2£Øg£©+2N2£Øg£©=8NO£Øg£©£»”÷H=+586 kJ•mol-1 | |
| D£® | ČōÓƱź×¼×“æöĻĀ4.48LCH4°ŃNO2»¹ŌĪŖN2£¬Õūøö¹ż³ĢÖŠ×ŖŅĘ1.6molµē×Ó |
·ÖĪö A£®øł¾ŻCŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĄ“¼ĘĖć×ŖŅʵĵē×Ó£»
B£®ÓÉĘųĢ¬Ė®±äĪŖŅŗĢ¬£¬·Å³öČČĮ棻
C£®øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł-¢ŚæɵĆ4NO2£Øg£©+2N2£Øg£©=8NO£Øg£©£»”÷H=+586 kJ•mol-1£»
D£®øł¾ŻøĒĖ¹¶ØĀÉ£¬$\frac{¢Ł+¢Ś}{2}$æɵĆCH4£Øg£©+2NO2£Øg£©=CO2£Øg£©+2H2O£Øg£©+N2£Øg£©£¬1molCH4·“Ó¦×ŖŅĘ8molµē×Ó£¬¾Ż“Ė¼ĘĖć£®
½ā“š ½ā£ŗA£®Į½øö·“Ó¦ÖŠ£¬CŌŖĖŲµÄ»ÆŗĻ¼Ū¾łÓÉ-4¼ŪÉżøßµ½+4¼Ū£¬ŌņµČĪļÖŹµÄĮæµÄ¼×Ķé·Ö±š²Ī¼Ó·“Ó¦¢Ł”¢¢Ś£¬·“Ó¦×ŖŅʵĵē×ÓŹżĻąĶ¬£¬¹ŹAÕżČ·£»
B£®ÓÉCH4£Øg£©+4NO2£Øg£©=4NO£Øg£©+CO2£Øg£©+2H2O£Øg£©”÷H=-574kJ•mol-1£¬Ė®ÓÉĘųĢ¬±äĪŖŅŗĢ¬£¬·Å³öČČĮ棬ŌņCH4£Øg£©+4NO2£Øg£©=4NO£Øg£©+CO2£Øg£©+2H2O£Øl£©”÷H=-Q£¬Q£¾574kJ•mol-1£¬ĖłŅŌ”÷H£¼-574 kJ•mol-1£¬¹ŹB“ķĪó£»
C£®øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł-¢ŚæɵĆ4NO2£Øg£©+2N2£Øg£©=8NO£Øg£©£»”÷H=+586 kJ•mol-1£¬¹ŹCÕżČ·£»
D£®øł¾ŻøĒĖ¹¶ØĀÉ£¬$\frac{¢Ł+¢Ś}{2}$æɵĆCH4£Øg£©+2NO2£Øg£©=CO2£Øg£©+2H2O£Øg£©+N2£Øg£©”÷H=-867kJ/mol£¬Ōņ1molCH4·“Ó¦×ŖŅĘ8molµē×Ó£¬ŌņÓƱź×¼×“æöĻĀ4.48LCH4»¹ŌNO2ÖĮN2£¬Õūøö¹ż³ĢÖŠ×ŖŅʵĵē×Ó×ÜŹżĪŖ0.2mol”Į8=1.6mol£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·“Ó¦¼°øĒĖ¹¶ØĀÉ£¬Ć÷Č·ČČ»Æѧ·“Ó¦µÄ¹ŲĻµ¼°ĪļÖŹµÄדĢ¬”¢·“Ó¦ČȵďżÖµÓėĪļÖŹµÄĮæµÄ¹ŲĻµ¼“æɽā“š£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĶŠÅĢĢģĘ½³ĘČ”3.2gNaCl¹ĢĢå | B£® | ÓĆ10mLĮæĶ²ĮæČ”7.5mLĻ”ŃĪĖį | ||
| C£® | ÓĆ450mLµÄČŻĮæĘæÅäÖĘ450mLČÜŅŗ | D£® | ÓĆ¹ć·ŗpHŹŌÖ½²āµĆijČÜŅŗµÄpHĪŖ3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
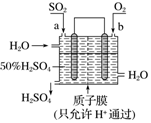
| A£® | aĪŖÕż¼«£¬bĪŖøŗ¼« | |
| B£® | Éś²ś¹ż³ĢÖŠĒāĄė×ÓÓÉÓŅŅĘĻņ×ó | |
| C£® | “Ó×óĻĀæŚĮ÷³öµÄĮņĖįµÄÖŹĮæ·ÖŹżŅ»¶Ø“óÓŚ50% | |
| D£® | øŗ¼«·“Ó¦Ź½ĪŖSO2+2H2O-2e-ØTSO42-+4H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōĶ | B£® | ĻõĖį¼Ų | C£® | ĀČ»ÆÄĘČÜŅŗ | D£® | ¶žŃõ»ÆĢ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 7ÖÖ | B£® | 8ÖÖ | C£® | 9ÖÖ | D£® | 10ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĘČ”12.5gµØ·ÆÅä³É500mLČÜŅŗ | B£® | ³ĘČ”8.0gµØ·ÆÅä³É500mLČÜŅŗ | ||
| C£® | ³ĘČ”8.0gĮņĖįĶ£¬¼ÓČė500mLĖ® | D£® | ³ĘČ”7.68gĮņĖįĶ£¬¼ÓČė500mLĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 12g½šøÕŹÆÖŠŗ¬¦Ņ¼üŹżĪŖ4 NA | |
| B£® | 1mol Na2O2¹ĢĢåÖŠŗ¬Ąė×Ó×ÜŹżĪŖ4 NA | |
| C£® | ag C2H4ŗĶC3H6µÄ»ģŗĻĪļĖłŗ¬Ģ¼Ēā¼üŹżÄæĪŖ$\frac{a{N}_{A}}{14}$ | |
| D£® | 30g¼×Č©ÖŠŗ¬¦Š¼üŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2ÄÜÓėĖ®·“Ó¦£¬ŌŚ·“Ó¦ÖŠCl2Ö»ÄÜ×÷Ńõ»Æ¼Į | |
| B£® | Ńõ»ÆŠŌCl2£¾Br2£¾I2£¬»¹ŌŠŌCl-£¾Br-£¾I- | |
| C£® | ŹµŃéŹŅÖʱøCl2£¬æÉÓĆÅű„ŗĶŹ³ŃĪĖ®¼ÆĘų·ØŹÕ¼Æ | |
| D£® | ĀČĖ®¾ßÓŠĖįŠŌ£¬æÉÓĆpHŹŌÖ½²āĮæĘäpHÖµ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”øßŅ»ÉĻ½Ģѧ֏¼ģ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
½«24.4 g NaOH¹ĢĢåČÜÓŚĖ®Åä³É100 mLČÜŅŗ£¬ĘäĆܶČĪŖ1.219 g”¤mL£1”£
£Ø1£©øĆČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ_______________”£
£Ø2£©øĆČÜŅŗÖŠNaOHµÄÖŹĮæ·ÖŹżĪŖ__________
£Ø3£©“ÓøĆČÜŅŗÖŠČ”³ö10 mL£¬ĘäÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ__________£¬NaOHµÄÖŹĮæ·ÖŹżĪŖ__________£¬ČÜŅŗµÄĆܶČĪŖ___________£¬ŗ¬NaOHµÄÖŹĮæĪŖ_________£¬ŗ¬NaOHµÄĪļÖŹµÄĮæĪŖ__________”£
£Ø4£©½«Č”³öµÄ10 mLČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½100 mL£¬Ļ”ŹĶŗóČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com