
【题目】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+比B3+多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E与C同主族且处于C的下两个周期。试回答:
(1)A是________(写元素符号),D是________(写元素名称).
(2)B的离子结构示意图________,A的单质分子的电子式__________,C元素最高价氧化物对应的水化物的电子式________。
(3)用电子式表示H2A形成过程:____________________。
(4)写出CD的溶液中通入氯气的离子方程式:_______________
(5)比较B、C、E三种元素形成的简单离子的半径大小:(B、C、E离子用实际离子符号表示) ________ > __________ > __________ 。
(6) 比较C 、E 两元素最高价氧化物对应的水化物的碱性强弱(用化学式表示)________ > __________。
【答案】O 碘 
![]()
![]()
![]() Cl2+2I-===2Cl-+I2 Cs+ K+ Al3+ CsOH KOH
Cl2+2I-===2Cl-+I2 Cs+ K+ Al3+ CsOH KOH
【解析】
现有A、B、C、D、E五种元素,它们的质子数依次增多.
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体,则A为氧元素;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱,则B为铝元素;
③B为铝元素,C+离子比B3+离子多8个电子,则C为钾元素;
④C与D元素可以形成化合物CD,
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色,则D为碘元素;
⑥C为钾元素,E、C同主族,且E比C多两个电子层,则E为Cs元素.
(1)A是O(写元素符号),D是碘(写元素名称)。
(2)B为铝元素,离子结构示意图 ,A是O,单质分子的电子式
,A是O,单质分子的电子式![]() ,C为钾元素,最高价氧化物对应的水化物KOH的电子式
,C为钾元素,最高价氧化物对应的水化物KOH的电子式![]() 。
。
(3)氧最外层6个电子,与氢形成2对共用电子对,用电子式表示H2A形成过程:![]() 。
。
(4)氯气能将碘离子氧化,KI的溶液中通入氯气的离子方程式:Cl2+2I-===2Cl-+I2
(5)B是铝元素,C为钾元素,D是铯元素,位于不同周期,离子的电子层数越多,半径越大,则有Cs+>K+>Al3+。
(6) 金属性Cs>K,C、E 两元素最高价氧化物对应的水化物的碱性强弱(用化学式表示) CsOH > KOH。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】科学家从化肥厂生产的(NH4)2SO4中检出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子,N4分子不能被植物吸收。
请回答下列问题:
(1)下列相关说法中,正确的是________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P-P键键能比N-N键能大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
(2)已知白磷、NH4+ 、N4H44+的空间构型均为四面体结构,参照NH4+和白磷的结构式,画出N4H44+的结构式(配位键用![]() 表示)________________;
表示)________________;
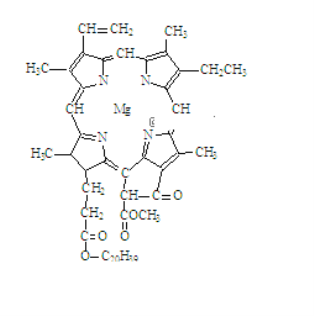
(3)在叶绿素结构示意图上标出N与Mg元素之间的配位键和共价键(配位键用![]() 表示)_______
表示)_______
(4)叠氮化物是研究较早的含全氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3)等。根据等电子体理论写出N3-的电子式_____________;叠氮化物能形成多种配合物,在[Co(N3)(NH3)5]SO4,其中钴显____价,它的配体是 ________________,写一种与SO42-等电子体的分子 ________________。
(5)六方相氮化硼晶体内B-N键数与硼原子数之比为_______,其结构与石墨相似却不导电,原因是_______________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按图1所示工艺流程制备氯化铜晶体(CuCl2·2H2O):
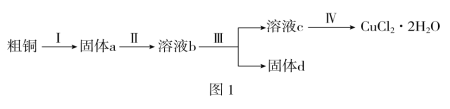
请回答下列问题:
(1)为了完成步骤Ⅰ,可采用图2所示的装置将粗铜完全转化为固体a:
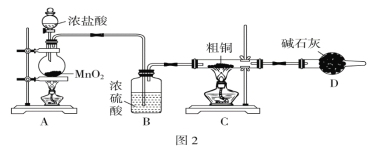
①A装置中发生反应的离子方程式是___________________________________________。
②在该实验中,点燃A、C装置中的酒精灯时,应该先点燃________装置的酒精灯,D装置的作用是_____________________________,C装置中生成的产物是________________。
③有同学认为应在B装置前增加吸收HCl的装置,你认为是否必要____(填“是”或“否”)。
(2)步骤Ⅱ的操作:将固体a置于烧杯中,然后加入_________,至固体完全溶解。
(3)步骤Ⅲ中应先加入某试剂调节溶液b的pH以除去杂质,该试剂可选用下列试剂中的________(填序号)。
a.NaOH溶液 b.氨水 c.CuO d.Cu2(OH)2CO3 e.CuSO4溶液
(4)步骤Ⅳ中,将溶液c蒸发浓缩、冷却结晶、过滤得到CuCl2·2H2O。现欲得到无水CuCl2,在实验室也可以采用图2所示装置使CuCl2·2H2O脱水得到无水CuCl2,则A装置中的两种化学试剂是___________________________(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鸦片具有复杂的组成,其中的罂粟碱的分子结构如图。鸦片最早用于药物(有止痛、止泻、止咳作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短。已知该物质的燃烧产物为CO2、H2O和N2,1 mol该化合物完全燃烧消耗O2的物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物同分异构体的种数分别是

A. 23.75 mol;5 B. 24.5 mol;7 C. 24.5 mol;8 D. 23.75 mol;4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)![]() 2NH3(g)
2NH3(g)
(1)已知每破坏1mol有关化学键需要的能量如下表:
H-H | N-H | N-N | N≡N |
435.9kJ | 390.8kJ | 192.8kJ | 945.8kJ |
(1)则反应物的总能量_________(填“>”或 “<”)生成物的总能量
(2)在一定温度下、向2L密闭容器中加入2 molN2、6 mol H2,在适当的催化剂作用下,发生反应 N2 (g)+3H2 (g)![]() 2NH3(g),10min后达到平衡,此时剩余4.5mol H2。
2NH3(g),10min后达到平衡,此时剩余4.5mol H2。
①下列叙述能说明此反应达到平衡状态的是____。
a.容器内总压强不变 b.v(H2)正=v(H2)逆 c.N2和H2的浓度相等
d. 2 mol NH3生成的同时有3 moH—H键断裂 e.NH3的浓度不再改变
②0~10 min内的平均反应速率v(H2) 是____mol/(Lmin);10秒末NH3的浓度是___mol/L;N2 的的物质的量___mol
Ⅱ.某温度时,在一个2L的密闭容器中X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,据此回答:

(1)该反应的化学方程式为___________
(2)从开始至2min,Z的平均反应速率为____________;
(3)改变下列条件,可以加快化学反应速率的有_________
A.升高温度 B.减小物质X的物质的量 C.减小压强 D.增加物质Z的物质的量. E.加入某种催化剂 F.缩小容积 G.使用效率更高的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按第26届国际计量大会重新定义,阿伏加德罗常数(NA)有了准确值6.02214076×1023。下列说法正确的是( )
A. 1mol乙烷中含有的共价键数目为6NA
B. 14g乙烯中含有的C-H键数目为2NA
C. 0.1molFe与0.1molCl2充分反应,转移的电子数月为0.3NA
D. 0.1molCH4与0.1molCl2经光照充分反应,生成CH3Cl的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向恒温恒容的密闭容器中充入H2(g)和I2(g)各0.1mol,发生反应H2(g)+I2(g)![]() 2HI(g),该反应的能量变化如图所示。下列说法正确的是( )
2HI(g),该反应的能量变化如图所示。下列说法正确的是( )

A. 该反应是吸热反应
B. 断裂0.05molH-H键和0.05molI-I键消耗的总能量小于生成0.1molH-I键释放的总能量
C. 当容器中气体密度不变时,说明反应已达到平衡状态
D. 达到平衡时,生成HI的分子数约为0.2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )

A. b为负极,发生还原反应
B. b电极反应式为2Fe3++2e-=Fe2+
C. 电子流动方向是a电极→FeCl3溶液→b电极
D. 电池的正极材料可以选用石墨、铂电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com