
【题目】对下列装置,不添加其他仪器无法检查装置气密性的是
A.  B.
B. 
C.  D.
D. 
【答案】B
【解析】检查装置气密性,必须使被检查装置形成密封体系。
A.用弹簧夹夹住右边导管,向长颈漏斗中倒水,若液面高度不变,说明装置气密性良好,所以能检查出装置是否漏气,选项A不选;B.图中的装置分液漏斗液面上的气体与烧瓶内气体相通,分液漏斗中的液体上下压强相等,所以无论该装置气密性是否良好,液体都会顺利滴下,所以不能检查出装置是否漏气,选项B选;C.图中的装置向外拉活塞,若气密性良好,则导管口会有气泡产生,若气密性不好则不会有气泡产生,所以能检查出装置是否漏气,选项C不选;D.对于该装置的气密性检查,主要是通过气体受热后体积膨胀、压强增大来进行检验.即用手握住试管外壁,如果装置漏气,压强不变化,就无现象;如果装置不漏气,温度升高,压强就变大就会在导管口产生气泡,所以能检查出装置是否漏气,选项D不选;答案选B。


科目:高中化学 来源: 题型:
【题目】已知:SO2+2H2O+I2=H2SO4+2HI; 向含SO32-、Fe2+、Br-、I-各0.1 mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图正确的是
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是
容器 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(H+) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
A. 该反应的逆反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表短周期的一部分
① | ||||||||
② | ③ | ④ | ||||||
⑤ | ⑥ | ⑦ | ⑧ | |||||
(1)①~⑦元素中金属性最强的元素是___________(用元素符号表示)。
(2)④与⑤形成的化合物的电子式为____________。
(3)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________(填化学式)。
(4)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为“![]() ”,该元素在元素周期表中的位置是_____________。
”,该元素在元素周期表中的位置是_____________。
(5)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液中:Fe3+、Mg2+、SCN–、Cl–
B. 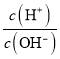 =1×1012的溶液中:K+、Na +、CO32-、NO3-
=1×1012的溶液中:K+、Na +、CO32-、NO3-
C. c(Fe2+) =1mol·L1的溶液中:K+、NH4+、MnO4-、SO42-
D. 能使甲基橙变红的溶液中:Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑料、合成橡胶和合成纤维这三大合成材料,都主要是以石油、煤和天然气为原料生产的,下列有关说法错误的是( )。
A.天然气作为化工原料主要用于合成氨和生产甲醇
B.煤可以直接液化,煤与氢气作用生成液体燃料
C.煤是以单质碳为主的复杂混合物,干馏时单质碳与混合的物质发生化学变化
D.聚乙烯塑料的主要成分聚乙烯是由乙烯通过聚合反应制得的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. NH4+、Al3+、Cl-、HCO3-在溶液中能大量共存
B. H2O2的电子式是:![]()
C. AlCl3溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
D. 铁锈是化合物,可用Fe2O3·nH2O(2<n<3)表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝鞣剂[主要成分为Al(OH)2Cl]主要用于鞣制皮革。利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂的一种工艺如图:
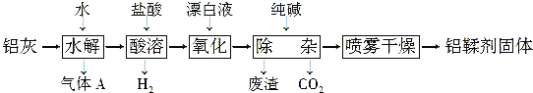
回答下列问题:
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90℃而不在室温下进行的原因是_________________ 。
(2)“酸溶”时,Al2O3发生反应的离子方程式为____________________。
(3)“氧化”时,发生反应的离子方程式为________________________。
(4)“除杂”时产生废渣的主要成分为____(填化学式),对其合理的处理方法是回收后制成___。
(5)准确称取所制备的铝鞣剂mg,将其置于足量硝酸中,待样品完全溶解后,加入足量AgNO3溶液,充分反应,过滤、洗涤、干燥得固体ng.则样品中Al(OH)2Cl的质量分数为____(用含m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在63Li 73Li 2311Na 2412Mg 146C 147N中
(1)_______和_______互为同位素
(2)_______和_______的质量数相等,但不能互称同位素
(3)_______和_______的中子数相等,但质子数不等,所以不属于同种元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com