
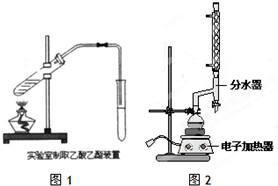
 ��ȩ�ڴ������ڵ������£����Ա��������������ᣮ���ݴ�ԭ�����ʵ���Ƶò����Թ�C���ռ�������������Һ����ͼ��ʾ���Թ�A��װ��40%����ȩˮ��Һ������ͭ��ĩ���Թ�C��װ����������ˮ���ձ�B��װ��ijҺ�壩����֪��60�桫80��ʱ��˫�����������������ɷ�����ȩ��������Ӧ����������ʮ���η�Ӧ������ȫ���й����ʵķе������
��ȩ�ڴ������ڵ������£����Ա��������������ᣮ���ݴ�ԭ�����ʵ���Ƶò����Թ�C���ռ�������������Һ����ͼ��ʾ���Թ�A��װ��40%����ȩˮ��Һ������ͭ��ĩ���Թ�C��װ����������ˮ���ձ�B��װ��ijҺ�壩����֪��60�桫80��ʱ��˫�����������������ɷ�����ȩ��������Ӧ����������ʮ���η�Ӧ������ȫ���й����ʵķе������| ���� | ��ȩ | ���� | ���� | �Ҷ��� | ˮ |
| �е� | 20.8�� | 117.9�� | 290�� | 197.2�� | 100�� |
���� ��1����ȩ����������������Ӧ�������
��2��ʵ�鿪ʼʱ�¶ȼ�Ӧ������Ӧ���¶ȣ����Ʒ�Ӧ�¶�Ϊ60�桫80�棻��������ԭ�����¶ȼƲ��������������¶ȣ�
��3������ķе�Ϊ117.9�棬Ҫ��ͨ������ķ����õ����ᣬB��ʢװ��Һ��ķе�Ӧ����117.9�棻
��4�����ͨ�������
��� �⣺��1����ȩ����������������Ӧ�������ᣬ����ʽΪ��2CH3CHO+O2$\stackrel{60��-80��}{��}$2CH3COOH��
�ʴ�Ϊ��2CH3CHO+O2$\stackrel{60��-80��}{��}$2CH3COOH��
��2��ʵ�鿪ʼʱ�¶ȼ�Ӧ������Ӧ���¶ȣ����Ʒ�Ӧ�¶�Ϊ60�桫80�棬����ʵ�鿪ʼʱ�¶ȼ�ˮ�����λ��Ӧ���Թ�A�ķ�ӦҺ�У�
������ԭ����֪���¶ȼƲ��������������¶ȣ������¶ȼ�ˮ�����λ��Ӧ���Թ�A��֧�ܿڴ���
�ʴ�Ϊ���Թ�A�ķ�ӦҺ�У����Ʒ�Ӧ�¶�Ϊ60�桫80�棻���Թ�A��֧�ܿڴ���
��3������ķе�Ϊ117.9�棬Ҫ��ͨ������ķ����õ����ᣬB��ʢװ��Һ��ķе�Ӧ����117.9�棬�ɱ���֪�ձ�B��ʢװ��Һ��������Ҷ�������ͣ�
�ʴ�Ϊ�����ͣ�
��4��������ʹPH��ֽ��죬��������̼�����Ʒ�ĩ��Ӧ�������ݣ����ɫʯ����ֽ��������Һ������ѡ��a��b���ʴ�Ϊ��ab��
���� ���������������Ʊ��������������ԭ������������ʣ���Ŀ�Ѷ��еȣ����ݿα�֪ʶ������ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| Ӧ��ȡŨ�������/mL | Ӧѡ������ƿ�Ĺ��/mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
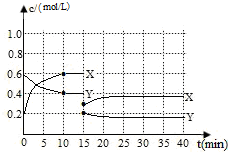 ��֪NO2��N2O4�����ת����2NO2��g��?N2O4��g����H��0���ֽ�һ����NO2��N2O4�Ļ������ͨ�����Ϊ1L�ĺ����ܱ������з���������Ӧ����Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��X��Y���������У�Y��ʾN2O4Ũ����ʱ��ı仯
��֪NO2��N2O4�����ת����2NO2��g��?N2O4��g����H��0���ֽ�һ����NO2��N2O4�Ļ������ͨ�����Ϊ1L�ĺ����ܱ������з���������Ӧ����Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��X��Y���������У�Y��ʾN2O4Ũ����ʱ��ı仯�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
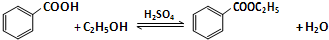
| ���� | ��ɫ״̬ | �ܶ�/g/cm3 | �۵�/�� | �е�/�� |
| ������ | ��ɫ���� | 1.2659 | 122 | 249 |
| ���������� | ��ɫҺ�� | 1.05 | -34.6 | 212.6 |
| ���� | ��ɫҺ�� | 1.0492 | 16.6 | 117.9 |
| �Ҵ� | ��ɫҺ�� | 0.789 | -117.3 | 78.5 |
| �������� | ��ɫҺ�� | 0.894-0.898 | -83.6 | 77.1 |
| ���� | ��ɫҺ�� | 0.713 | -116.3 | 34.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
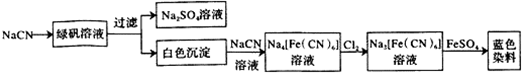
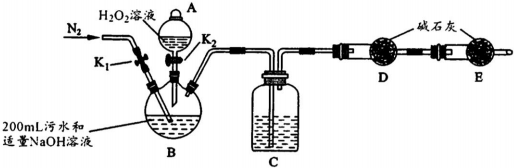
| ����1 | �ر�K1����K2����������H2O2��Һ����B���ȣ���ַ�Ӧ��ֹͣ���ȣ� |
| ����2 | ��ȴ����ע��������Bװ�õĽ���ע��ϡH2S04��Һ�� |
| ����3 | ��K1��ͨ��N2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
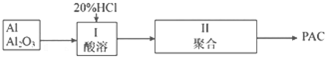
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
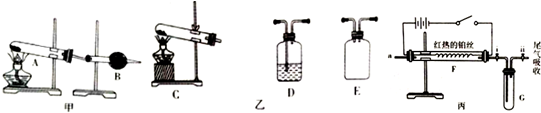
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 0.5 L����Һ�������ӵ����ʵ���Ũ��Ϊ0.1 mol/L | |
| B�� | 1 L����Һ�к���Na2CO3������Ϊ10.6 g | |
| C�� | ��1 L����Һ��ȡ��100 mL����ȡ����Һ��Na2CO3�����ʵ���Ũ��Ϊ0.01 mol/L | |
| D�� | ȡ����Һ10 mL����ˮϡ����100 mL��Na2CO3�����ʵ���Ũ��Ϊ0.01 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
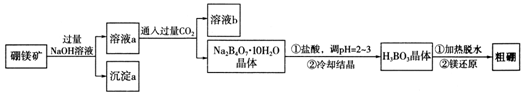

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com