
| A. | ②的溶液变黄的原因是反应产生Fe3+ | |
| B. | 上述实验中,共有两个氧化还原反应 | |
| C. | 实验①生成的气体不能使湿润的淀粉KI试纸变蓝 | |
| D. | 实验②证明Fe2+既有氧化性又有还原性 |
分析 ①向KMnO4晶体滴加浓盐酸,产生黄绿色气体,该反应中Mn元素化合价由+7价变为+2价、Cl元素化合价由-1价变为0价,高锰酸钾是氧化剂、浓盐酸是还原剂;
②向FeCl2溶液中通入少量氯气,溶液变黄色,铁元素化合价由+2价变为+3价、Cl元素化合价由0价变为-1价,氯化亚铁是还原剂、氯气是氧化剂;
③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色,铁离子和碘离子发生氧化还原反应生成碘和亚铁离子,I元素化合价由-1价变为0价、铁元素化合价由+3价变为+2价,所以碘离子作还原剂、铁离子为氧化剂,以此解答该题.
解答 解:A.向FeCl2溶液中通入少量氯气,溶液变黄色,铁元素化合价由+2价变为+3价,产生Fe3+,故A正确;
B.三个反应中均存在元素的化合价变化,均属于氧化还原反应,故B错误;
C.由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性:MnO4->Cl2>Fe3+>I2,可实验①生成的气体能使湿润的淀粉KI试纸变蓝,故C错误;
D.实验②中Fe元素的化合价升高,只可以证明Fe2+有还原性,故D错误.
故选A.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及分析与应用能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:推断题

 .
. .
.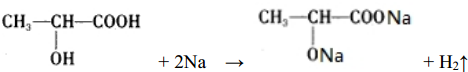 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O | |
| B. | 金属铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | FeCl2溶液和Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
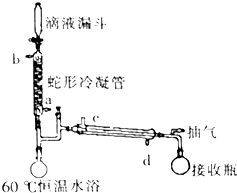 过氧乙酸是高效、速效、广谱灭菌剂.实验室合成与含量测定的相关步骤如下:
过氧乙酸是高效、速效、广谱灭菌剂.实验室合成与含量测定的相关步骤如下: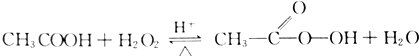 ,向装有搅拌装置及温度计的500ml三口烧瓶中先加入16.0g冰醋酸,然后在搅拌下滴加90g浓缩后的H2O2溶液,最后加入7.5ml浓硫酸,搅拌下加热5h,静置20h.
,向装有搅拌装置及温度计的500ml三口烧瓶中先加入16.0g冰醋酸,然后在搅拌下滴加90g浓缩后的H2O2溶液,最后加入7.5ml浓硫酸,搅拌下加热5h,静置20h.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L 16O 2和3.6 g 18O 2均含有0.2N A个氧原子 | |
| B. | 1.7 g H 218O 2中含有的电子数为0.9 N A | |
| C. | 电解精炼铜时,若阴极得到N A个电子,则阳极质量减少32g | |
| D. | 标准状况下,2.24 L甲烷、戊烷混合物所含分子数为0.1N A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com