
| A. | 0.2mol | B. | 0.4 mol | C. | 0.6 mol | D. | 0.8 mol |
分析 根据碳元素守恒V(CO2)=V(CH4)+V(CO)+2V(C2H6)=[V(CH4)+V(CO)+V(C2H6)]+V(C2H6)=8.96L+V(C2H6),据此计算原混合气体中C2H6的体积,再根据n=$\frac{V}{{V}_{m}}$计算出混合气体中C2H6的物质的量.
解答 解:根据碳元素守恒可知:V(CO2)=V(CH4)+V(CO)+2V(C2H6),则:17.92LL=[V(CH4)+V(CO)+V(C2H6)]+V(C2H6)=8.96L+V(C2H6),原混合气体中V(C2H6)=17.92L-8.96L=8.96L,
则原混和气体中含C2H6的物质的量为:$\frac{8.96L}{22.4L/mol}$=0.4mol,
故选B.
点评 本题考查混合物的有关计算,题目难度中等,根据体积变化确定原混合气体中C2H6的体积是关键,也可以利用差量法计算,试题培养了学生分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | CaO失氧变为CaC2 | B. | C的状态发生了变化 | ||
| C. | Ca的化合价在反应前后发生了改变 | D. | C失去了电子,同时也得到了电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用润湿的pH试纸测定0.1mol/L氨水的pH值 | |
| B. | 在CaCO3饱和溶液中,加入Na2CO3固体,平衡时c(Ca2+)=c(CO${\;}_{3}^{2-}$)=$\sqrt{{K}_{sp}CaC{O}_{3}}$ | |
| C. | 图I装置可用于探究浓度对化学反应速率的影响 | |
| D. | 观察图II导管中水柱的变化,可知该条件下铁钉主要发生了析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,电离能(I)数据依次为:I1=490kJ/mol-1,I2=4562kJ/mol-1,I3=6912kJ/mol-1… |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 在第四周期元素原子中,其所含不成对电子数最多 |
 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1.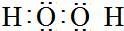 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热反应,升高反应的温度,反应速率减慢 | |
| D. | 用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,反应速率可能减小 | |
| B. | 需要加热的反应一定为吸热反应 | |
| C. | 使用催化剂不能使化学平衡发生移动 | |
| D. | 使某金属做电解池的阳极,可使该金属得到有效的保护 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5、5、10、10 | B. | 4、4、10、10 | C. | 3、5、11、9 | D. | 5、3、9、11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com