
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是![]()
A.白磷![]() 为正四面体结构,则
为正四面体结构,则![]() 与
与![]() 所含共价键数目之比为3:1
所含共价键数目之比为3:1
B.1mol乙酸与足量的![]() 充分发生酯化反应可生成
充分发生酯化反应可生成![]() 分子
分子![]() 个
个
C.![]() 与
与![]() 的混合物中所含中子数为
的混合物中所含中子数为![]()
D.浓度均为![]() 的醋酸和醋酸钠溶液等体积混合,溶液中
的醋酸和醋酸钠溶液等体积混合,溶液中![]() 和
和![]() 的总数为
的总数为![]()
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。
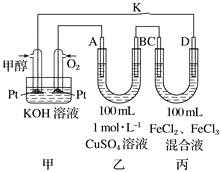
(1)写出甲池中负极电极反应式_________________________________________
(2)写出A电极的电极反应式____________________________________________
(3)写出丙中反应的离子方程式___________________________________________
(4)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。则乙中A极析出的气体在标准状况下的体积为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见有机物 A、B、C、D、E的相互转化关系如下图。已知D 是有香味且不易溶于水的油状液体,E的产量可以用来衡量一个国家的石油化工发展水平。
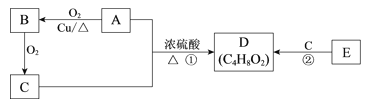
请回答:
(1)A中含有的官能团名称是___________。
(2)B的结构简式是___________。
(3)①的化学方程式是__________________。
(4)下列说法正确的是______。
a.E分子中所有原子在同一平面上
b.用饱和Na2CO3溶液除去D中混有的C
c.②的反应类型为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000mol·L-1的NaOH溶液滴定20.00mL浓度为0.1000mo l·L-1的某酸HX,滴定曲线如图所示。下列说法正确的是( )

A. HX的电离常数Ka的数量级为10-10
B. P点溶液中微粒浓度大小为:c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+)
C. 滴定过程中可选用的指示剂有甲基橙和酚酞
D. A点到B点过程中,水电离出的c(H+)×c(OH-)先增大,后不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为_______________________________________。
(2)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=________。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为_____________________。
(4)若0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=_______________mol·L-1(填精确计算结果)。
(5) 将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L 1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度由大到小的顺序为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入![]() 溶液,所加NaOH溶液的体积
溶液,所加NaOH溶液的体积![]() 与产生沉淀的物质的量
与产生沉淀的物质的量![]() 关系如下图所示,下列说法不正确的是
关系如下图所示,下列说法不正确的是 ![]()
![]()
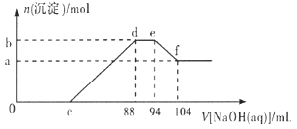
A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.c点对应溶液的体积为![]()
C.b点与a点的差值为![]()
D.样品中铝粉和铁粉的物质的量之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠哟哟因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖。青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
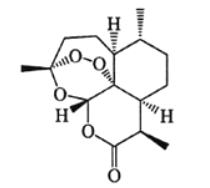
A.可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结构
B.提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙酸进行萃取
C.青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性
D.元素分析仪可以确定青蒿素中是否含有C、H、O等元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分子组成表示为CxHy的烷、烯、炔烃说法不正确的是( )
A.当x≤4时,均为气体(常温常压下)
B.y一定是偶数
C.分别燃烧1mol,消耗氧气(x+![]() )mol
)mol
D.在容积固定密闭容器中完全燃烧,反应前后均150℃时测得的压强一定是反应后大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是( )
A.甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=890.3 kJ/mol
B.取50mL 0.55mol/L NaOH(aq)和50mL 0.50mol/L HCl(aq)进行中和热的测定实验,用温度计测定HCl(aq)起始温度后,直接测定NaOH(aq)的温度,会使中和热ΔH偏小
C.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D.已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O2比O3稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com