
| A. | 10mL 0.1mol/L Na2S2O3中加入10mL0.1mol/L H2SO4 | |
| B. | 5mL 0.1mol/L Na2S2O3中加入5 mL0.1mol/L H2SO4 | |
| C. | 5mL 0.1mol/L Na2S2O3中加入10mL0.05mol/L H2SO4 | |
| D. | 10mL 0.05mol/L Na2S2O3中加入10mL0.1mol/L H2SO4 |
分析 发生反应:S2O32-+2H+=S↓+SO2↑+H2O,计算混合后为反应时S2O32-、H+的浓度,温度下相同条件下,浓度越大反应速率愉快.
解答 解:A.混合后为反应时c(S2O32-)=$\frac{0.1mol}{2}$=0.05mol/L,c(H+)=$\frac{0.1mol/L×2}{2}$=0.1mol/L;
B.混合后为反应时c(S2O32-)=$\frac{0.1mol}{2}$=0.05mol/L,c(H+)=$\frac{0.1mol/L×2}{2}$=0.1mol/L;
C.混合后为反应时c(S2O32-)=$\frac{0.1mol/L×5}{5mL+10mL}$=0.033mol/L,c(H+)=$\frac{0.05mol/L×2×10mL}{(5mL+10mL)}$=0.067mol/L;
D.混合后为反应时c(S2O32-)=0.05mol/L×$\frac{1}{2}$=0.025mol/L,c(H+)=0.05mol/L×2×$\frac{1}{2}$=0.05mol/L,
D中S2O32-、H+的浓度均最小,相同温度下,D中反应速率最小,
故选D.
点评 本题考查难度对反应速率的影响,难度不大,注意利用混合后未反应时的浓度,不是混合前各物质的浓度.


科目:高中化学 来源: 题型:解答题
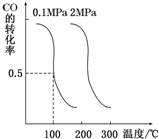 随着能源与环境问题越来越被人们关注,碳一化学成为研究的热点.“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学工艺.
随着能源与环境问题越来越被人们关注,碳一化学成为研究的热点.“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学工艺.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 表现了氧化性 | B. | 表现了还原性 | ||
| C. | 既表现了氧化性又表现了还原性 | D. | 既不表现氧化性也不表现还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com