
【题目】下列有关电解质溶液中粒子浓度关系正确的是( )
A.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
B.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
C.常温下,0.1molL-1的①NH4Cl②CH3COONH4③NH4HSO4溶液中:c(NH4+)大小顺序:①>②>③
D.物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-)
【答案】B
【解析】
A.含有AgCl和AgI固体的悬浊液,碘化银的溶解度小于氯化银,则氯离子浓度大于碘离子,溶液中离子浓度大小为:![]() ,故A错误;
,故A错误;
B.![]() 是强电解质,完全电离生成钠离子、氢离子和硫酸根离子,根据电荷守恒,
是强电解质,完全电离生成钠离子、氢离子和硫酸根离子,根据电荷守恒,![]() 的
的![]() 溶液存在:
溶液存在:![]() ,因为
,因为![]() ,所以
,所以![]() ,故B正确;
,故B正确;
C.NH4HSO4可电离生成铵根离子、氢离子、硫酸根离子,铵根离子水解,c(NH4+)减小,其溶液中![]() 抑制
抑制![]() 水解、H3COONH4溶液中
水解、H3COONH4溶液中![]() 促进
促进![]() 水解,所以铵根离子浓度大小顺序是
水解,所以铵根离子浓度大小顺序是![]() ,故C错误;
,故C错误;
D.根据物料守恒,NaClO溶液中存在c(HClO)+c(ClO-)= c(Na+),NaHCO3溶液中存在c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),物质的量浓度之比为1:2的NaClO和NaHCO3溶液中,NaHCO3溶液中钠离子的浓度是NaClO溶液中钠离子的浓度的两倍,则有![]() ,故D错误;
,故D错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】H2CO3是一种二元弱酸,常温下H2CO3水溶液中碳元素的存在形态的物质的量分数与溶液的pH的关系如图所示,据此分析,下列说法不正确的是( )
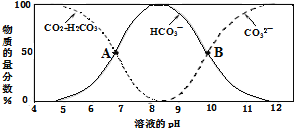
A.pH=8时,溶液中含碳元素的微粒主要是HCO3—
B.A点,溶液中H2CO3和HCO3-浓度相同
C.当c(HCO3-)=c(CO32-)时,c(H+)<c(OH-)
D.pH=8.4的水溶液中加入NaOH溶液时,发生反应的离子方程式可为:HCO3-+OH-=CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ ![]() O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ ![]() O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
A.①B.④C.②③④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图中各装置的叙述正确的是( )

A.装置①可制备少量氧气
B.装置②可用于实验室制取和收集乙酸乙酯
C.装置③的实验可推断硫、碳、硅三种元素的非金属强弱
D.装置④能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:

(1)电解质由强至弱顺序为___(用化学式表示,下同)。
(2)常温下,0.02mol·L-1的CH3COOH溶液的电离度约为___,体积为10 mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者___后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____。
(4)NaHSO3溶液显酸性的原因_____(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镉镍可充电电池的充、放电反应按下式进行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,由此判断,下列说法错误的是
Cd(OH)2+2Ni(OH)2,由此判断,下列说法错误的是
A. 放电时,NiO(OH)作正极
B. 放电时,Cd发生还原反应
C. 电解质溶液为碱性溶液
D. 充电时,阳极反应为Ni(OH)2+OH--e-== NiO(OH)+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半,下列说法正确的是( )
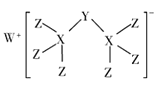
A.氧化物对应的水化物的酸性:Z> Y> X
B.元素X可与元素W形成化合物W2X,该化合物与水能产生可燃气体
C.该新化合物中Y不满足8电子稳定结构
D.Z氢化物的沸点一定比X氢化物的佛点高.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:
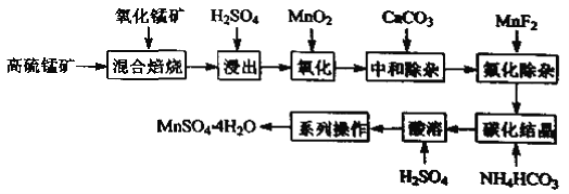
已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中的平衡浓度与pH的关系如图所示(25℃):
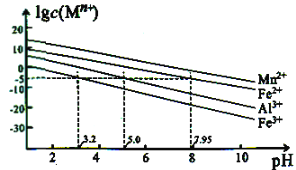
③此实验条件下Mn2+开始沉淀的pH为7.54;当离子浓度≤105mol·L1时,可认为离子沉淀完全。
请回答:
(1)传统工艺处理高硫锰矿时,不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为____。
(2)“氧化”时,发生反应的离子方程式为____。若省略“氧化”步骤,造成的后果是____。
(3)“中和除杂”时,生成沉淀的主要成分为____(填化学式)。
(4)“氟化除杂”时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于____。(已知:Ksp(MgF2)=6.4×1010;Ksp(CaF2)=3.6×1012)
(5)“碳化结晶”时,发生反应的离子方程式为_____。
(6)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为四种短周期元素,它们的原子序数依次增大。A与其他几种元素均不在同一周期;B元素最高价氧化物对应的水化物能与其最简单氢化物反应生成一种盐X;C能形成两种常温下为液态的氢化物;D与C同主族。则下列说法中不正确的是( )
A.原子半径大小关系:A<C<B
B.在0.1molL-1的X溶液中,溶液中阳离子的数目小于0.1NA
C.C、D两种元素分别与A形成的最简单化合物的沸点C比D的要高
D.化合物X受热易分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com