
下列有关离子检验的方法正确的是
A.NH4+:加NaOH溶液,加热,滴入酚酞溶液检验所得溶液
B.CO32-:加入稀盐酸,产生无色能使澄清石灰水变浑浊的气体
C.Fe3+:加入KSCN溶液,溶液呈血红色
D.Cl-:加入AgNO3溶液,产生白色沉淀
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源:2016届辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
等量的铝,分别与足量的盐酸和氢氧化钠溶液充分反应,放出的氢气在同温同压下的体积比为
A.1:3 B.1:6 C.1:1 D.2:3
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高一上学期期中考试化学试卷(解析版) 题型:选择题
若1gN2含a个分子,则阿伏加德罗常数可表示为
A.a/28mol-1 B.a mol-1 C.28a mol-1 D.a/14 mol-1
查看答案和解析>>
科目:高中化学 来源:2016届福建省龙岩市高一第一学期教学质量检测化学试卷(解析版) 题型:选择题
下列实验现象的叙述,正确的是
A.钠在氧气中燃烧,火焰呈黄色,产生白色固体
B.氢气在氯气中燃烧,发出苍白色火焰,同时产生白烟
C.钠投入水中,将沉在水底并熔化成小球、且有气泡产生
D.氯气通入紫色石蕊试液中,溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源:2016届福建省宁德市高一上学期期末考试化学试卷(A)(解析版) 题型:实验题
某研究性学习小组的同学想通过下图实验装置探究SO2与Na2O2反应的产物。(夹持装置已略去,装置的气密性良好)
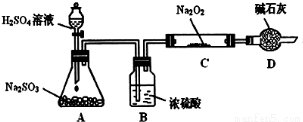
Ⅰ.实验中装置B可吸收水分,干燥SO2气体,其目的是:_________________________。
装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是:_________________。
Ⅱ.对C中固体产物提出如下假设:(假设Na2O2已全部反应)
假设1:__________。 假设2:只有Na2SO4; 假设3:既有Na2SO3又有Na2SO4。
(1)甲同学认为SO2与Na2O2的反应不同于CO2,应为假设2成立,请据此写出C中所发生反应的化学方程式:_____________________。
(2)若假设2成立,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:C中固体产物只有Na2SO4。该方案是否合理?答:__________。(填“是”或“否”)理由是______________________________。
(3)乙同学为证明假设3成立,设计如下实验。
实验步骤和结论为:
①取少量C中固体产物于试管中,加入适量的蒸馏水溶解;
②滴加过量的1mol?L-1BaCl2溶液,若产生白色沉淀,则证明C中固体产物中有_________;
③滴加适量的1mol?L-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,则证明C中固体产物中有___________________。
查看答案和解析>>
科目:高中化学 来源:2016届福建省宁德市高一上学期期末考试化学试卷(A)(解析版) 题型:选择题
下列离子方程式书写正确的是
A.盐酸与碳酸钡反应:CO32-+2H+=CO2↑+H2O
B.往硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-= BaSO4↓+Cu(OH)2↓
C.稀硫酸溶液与氨水反应:H++OH-=H2O
D.铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源:2016届福建省宁德市高一上学期期末考试化学试卷(A)(解析版) 题型:选择题
除去混在Na2CO3粉末中的少量NaHCO3,下列最合理的方法是
A.加入适量NaOH溶液 B.加热到固体质量不变
C.加入适量HCl溶液 D.加入适量CaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.铁与稀硝酸反应:Fe+2H+=Fe2++H2↑
B.用氨水吸收少量的SO2: NH3·H2O +SO2=NH4++HSO3-
C.用小苏打治疗胃酸过多:HCO3-+H+ = CO2↑+H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu = Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源:2016届福建省高一上学期期中考试化学试卷(解析版) 题型:实验题
用质量分数为98%,密度为1.84g· cm-3的浓硫酸配制250mL物质的量浓度为2mol·L-1的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、 、 。
(2)其操作步骤可分解为以下几步:
A.用量筒量取 mL浓硫酸, (简述浓硫酸的稀释操作),冷却
B.用蒸馏水洗涤烧杯和玻璃棒2~3次,将每次的洗涤液都转移入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流至容量瓶里
D.检查250mL容量瓶是否漏水
E.将蒸馏水直接加入容量瓶至刻度线以下2cm处
F.盖紧瓶塞,上下倒转摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到凹液面最低点恰好与刻度线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
( )→( )→( )→ B →( )→( )→( )
③进行A步操作时,选用量筒的规格是 。(选填字母)
A.10mL B.50mL C.100mL D.1000mL
④下列情况对所配制的稀硫酸浓度有何影响?(选填“偏高”、“偏低”、“无影响”)。
A.用量筒量取浓硫酸时仰视,配制的稀硫酸浓度将
B.容量瓶用蒸馏水洗涤后残留有少量的水_________
C.定容时仰视溶液的凹液面 _________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com