
 已知:苯酚(
已知:苯酚(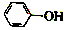 )在水中的电离方程式为
)在水中的电离方程式为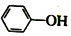 ?
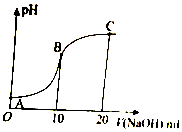
?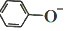 +H+,25℃时,苯酚的电离常数Ka=1.0×10-10.25℃时,用0.0100mol•L-1的NaOH溶液滴定20.00mL0.0100mol•L-1的苯酚溶液,溶液的pH与所加NaOH溶液的体积(V)的关系如图所示.下列说法正确的是( )
+H+,25℃时,苯酚的电离常数Ka=1.0×10-10.25℃时,用0.0100mol•L-1的NaOH溶液滴定20.00mL0.0100mol•L-1的苯酚溶液,溶液的pH与所加NaOH溶液的体积(V)的关系如图所示.下列说法正确的是( )| A. | A点溶液中,苯酚的电离度约为0.01% | |
| B. | B点溶液的pH<7 | |
| C. | C点溶液中存在c(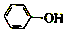 )>c(OH-)>c(H+) )>c(OH-)>c(H+) | |
| D. | A 点溶液加少量水稀释,溶液中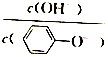 减小 减小 |
分析 A.设苯酚电离出氢离子浓度为x,则 的浓度为x,苯酚的浓度约为为0.0100mol•L-1,然后结合Ka=1.0×10-10计算;
的浓度为x,苯酚的浓度约为为0.0100mol•L-1,然后结合Ka=1.0×10-10计算;
B.B点反应溶质为等浓度的苯酚和苯酚钠,混合液酸碱性取决于苯酚的电离程度与 水解程度大小;
水解程度大小; 水解平衡常数Kh=$\frac{{K}_{W}}{{K}_{a}}$,根据水解平衡常数和电离平衡常数大小判断溶液酸碱性;
水解平衡常数Kh=$\frac{{K}_{W}}{{K}_{a}}$,根据水解平衡常数和电离平衡常数大小判断溶液酸碱性;
C.C点溶质为苯酚钠,氢氧根离子来自苯酚钠的水解和水的电离,则c(OH-)>c( );
);
D.根据 水解平衡常数可知:
水解平衡常数可知: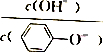 =$\frac{K}{c(苯酚)}$,结合稀释过程中苯酚的电离程度增大分析.
=$\frac{K}{c(苯酚)}$,结合稀释过程中苯酚的电离程度增大分析.
解答 解:A.设苯酚电离出氢离子浓度为x,则 的浓度为x,苯酚的浓度约为为0.0100mol•L-1,Ka=1.0×10-10=$\frac{x×x}{0.01}$,解得:x=1.0×10-6mol/L,A点溶液中苯酚的电离度约为:$\frac{1×1{0}^{-6}}{0.01}$×100%=0.01%,故A正确;
的浓度为x,苯酚的浓度约为为0.0100mol•L-1,Ka=1.0×10-10=$\frac{x×x}{0.01}$,解得:x=1.0×10-6mol/L,A点溶液中苯酚的电离度约为:$\frac{1×1{0}^{-6}}{0.01}$×100%=0.01%,故A正确;
B.B点加入10mLNaOH溶液,反应后溶质为等浓度的 和苯酚钠,
和苯酚钠, 水解平衡常数Kh=$\frac{{K}_{W}}{{K}_{a}}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-10}}$=1.0×10-4>1.0×10-6mol,说明
水解平衡常数Kh=$\frac{{K}_{W}}{{K}_{a}}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-10}}$=1.0×10-4>1.0×10-6mol,说明 的水解程度大于
的水解程度大于 的电离程度,混合液呈碱性,溶液的pH>7,故B错误;
的电离程度,混合液呈碱性,溶液的pH>7,故B错误;
C.C点加入20mLNaOH溶液,反应后溶质为苯酚钠, 水解溶液呈碱性,由于氢氧根离子来自水的电离和
水解溶液呈碱性,由于氢氧根离子来自水的电离和 的水解,则(OH-)>c(
的水解,则(OH-)>c( ),溶液中正确的离子浓度大小为:c(OH-)>c(
),溶液中正确的离子浓度大小为:c(OH-)>c( )>c(H+),故C错误;
)>c(H+),故C错误;
D.设 的水解平衡常数为K,则
的水解平衡常数为K,则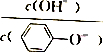 =$\frac{K}{c(苯酚)}$,由于稀释过程中苯酚的电离程度增大,溶液中苯酚浓度减小,则该比值逐渐增大,故D错误;
=$\frac{K}{c(苯酚)}$,由于稀释过程中苯酚的电离程度增大,溶液中苯酚浓度减小,则该比值逐渐增大,故D错误;
故选A.
点评 本题考查弱电解质的电离平衡及其影响、离子浓度大小比较,题目难度中等,明确弱电解质的电离特点为解答关键,注意掌握盐的水解原理,试题培养了学生的分析能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 正极 | Zn | Ag | Cu | Cu |
| 负极 | Cu | Cu | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | FeCl2 | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )| A. | B极区电解液为LiOH溶液 | |
| B. | 每产生标准状况下2.24L氢气,就有0.1 mol阳离子通过交换膜进入阴极区 | |
| C. | 电解过程中Li+向B电极迁移 | |
| D. | 阳极电极反应式为2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,Zn2+向ZnMn2O4电极迁移 | |
| B. | 充电时,阳极反应:ZnMn2O4-2xe-═Zn1-xMn2O4+xZn2+ | |
| C. | 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g | |
| D. | 充放电过程中,只有Zn元素的化合价发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| B. | 在水溶液中能导电的化合物一定是离子化合物 | |
| C. | 共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏 | |
| D. | 含有离子键的物质不可能是单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属:S>C |
| B | 向雨水中加入少量硫酸铁 | 容器底部出现不溶物 | 铁盐具有杀菌作用 |
| C | 向蔗糖中加入浓H2SO4 | 蔗糖变黑,并放出有刺激性气味的气体 | 浓H2SO4具有脱水性 |
| D | 有色布条放入盛满干燥的Cl2的集气瓶中,盖上玻璃片 | 布条不褪色 | 干燥的Cl2不能漂白 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在食品袋中放入CaCl2•6H2O,可防止食物受潮 | |
| B. | “从沙滩到用户”,计算机芯片的材料是指单质硅 | |
| C. | 二氧化硫有毒,严禁将其添加到任何食品和饮料中 | |
| D. | 用Al(OH)3可以做塑料的阻燃剂,因为它受热熔化放出大量的热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在12.0g NaHSO4晶体中,所含离子数目为0.3NA | |
| B. | 在1.0L 1.0mol/L的NaA1O2溶液中,含有的氧原子数为2NA | |
| C. | 将1molCl2通入足量水中,转移电子数为NA | |
| D. | 常温常压下,2.2gC O2和N2O的混合气体含有的电子数为1.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于△S>0的反应,若在任何温度下均能自发进行,则该反应△H>0 | |
| B. | 铅蓄电池放电时的负极和充电时的阳极均发生在原反应 | |
| C. | 水解NH4++H2O?NH3•H2O+H+反应达到平衡后,升高温度平衡逆向移动 | |
| D. | 等体积、等物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com