
| m |
| M |
| V |
| Vm |
| 11.2L |
| 22.4L/mol |
| 8.4g |
| 28g/mol |


科目:高中化学 来源: 题型:
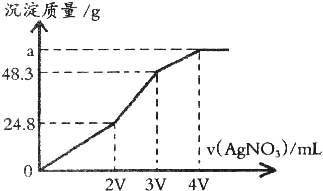
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用氢氟酸来刻蚀玻璃器皿 |
| B、用活性炭去除冰箱中的异味 |
| C、用煤液化和气化得到清洁燃料 |
| D、用热碱溶液清除炊具上残留的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:
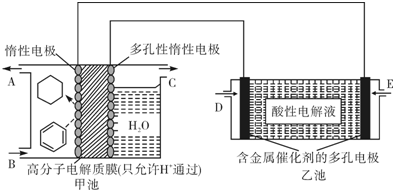
| A、乙池中溶液的pH变大 |
| B、E处通入H2,C处有O2放出 |
| C、甲池中阴极区只有苯被还原 |
| D、导线中共传导11.2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
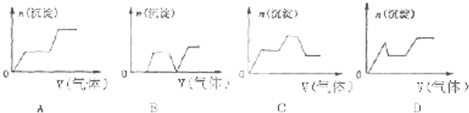
| t/min | 0 | 5 | 10 |
| AO/mol?L-1 | 1.00 | 0.65 | 0.50 |
| H2/mol?L-1 | 2.00 | 1.00 | |
| AH3OH/mol?L-1 | 0.00 | 0.35 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 | ||
| B、水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 | ||
C、往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中
| ||
| D、等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3⑤NH4HCO3中c(CO32-)的大小关系为:②>④>③>⑤>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| CH3C=CNa |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com