
| A. | 颜色变浅 | B. | 逐渐变深绿 | C. | 没有改变 | D. | 变棕黄色 |
科目:高中化学 来源: 题型:解答题
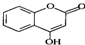 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成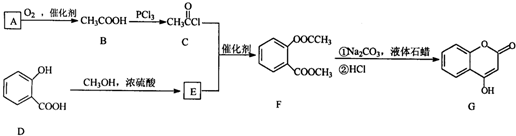
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性 | |
| B. | 乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性 | |
| C. | 乙醇与钠反应可以产生氢气,所以乙醇显酸性 | |
| D. | 乙醇与钠反应时,乙醇羟基上的氢原子被置换 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某同学在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图中A、B、C、D分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中不正确的是( )
某同学在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图中A、B、C、D分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中不正确的是( )| A. | 紫色 | B. | 蓝色 | C. | 红色 | D. | 无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
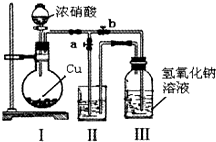 针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物油不能发生水解反应 | |
| B. | 淀粉水解的最终产物是麦芽糖 | |
| C. | 蔗糖水解产物只有葡萄糖 | |
| D. | 蛋白质溶液遇CuSO4后产生的沉淀置于水中不能重新溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
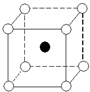 如图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子.已知晶体中2个最近的铯离子的核间距离为a cm,氯化铯的摩尔质量为M g/mol,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子.已知晶体中2个最近的铯离子的核间距离为a cm,氯化铯的摩尔质量为M g/mol,则氯化铯晶体的密度为( )| A. | $\frac{2M}{{N}_{A}{a}^{3}}$g/cm3 | B. | $\frac{M}{2{N}_{A}{a}^{3}}$g/cm3 | C. | $\frac{M}{{N}_{A}{a}^{3}}$g/cm3 | D. | $\frac{M{a}^{3}}{{N}_{A}}$g/cm3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com