
【题目】下列金属元素的单质或化合物在火焰上灼烧时,焰色为紫色的是
A. 钠 B. 钾 C. 镁 D. 铁
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 最外层电子数是电子层数的两倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X的一种同位素可测定文物年代,该核素的原子核内有8个中子,则这种同位素的符号是________。
(2)元素Y的单质的电子式为_________________,元素Y和元素Z可形成一种各原子最外层均为8电子结构的化合物,该化合物的结构式为 ___________
(3)元素X与元素T相比,非金属性较强的是元素T,下列表述中不能证明这一事实的选项是_____。
a.常温下元素X的单质和元素T的单质的熔沸点不同
b.元素T的氢化物比元素X的氢化物稳定
c.元素X和元素T的单质都能在氧气中燃烧
d.元素T最高价氧化物对应水化物的酸性比元素X最高价氧化物对应水化物的酸性强
e.Na2XO3溶液呈碱性,Na2TO4溶液呈中性
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中,化学性质明显不同于其他三种酸的是_______________(用化学式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 3.6 g 碳在 6.4 g 的氧气中燃烧,至反应物耗尽,并放出 X kJ 热量。已知单质 C(s)的燃烧热数值为 Y kJ·mol-1,则 1 mol C(s)与 O2(g)反应生成 CO(g)的反应热 ΔH 为( )
A. -Y kJ/mol B. -(10X-Y) kJ/mol C. -(5X-0.5Y) kJ/mol D. +(10X-Y) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.58kJ·mo1-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mo1-1
反应Ⅱ:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g) ![]() CH3OH(g) △H3=-90.77 kJ·mo1-1
CH3OH(g) △H3=-90.77 kJ·mo1-1
回答下列问题:
(1)反应Ⅱ的△H2=__________。
(2)反应Ⅲ能够自发进行的条件是__________(填“较低温度”、“较高温度”或“任何温度”)。
(3)恒温,恒容密闭容器中,对于反应I,下列说法中能说明该反应达到化学平衡状态的是__________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1︰3︰1︰1
D.甲醇的百分含量不再变化
(4)对于反应I,温度对CO2的转化率及催化剂的效率影响如图所示:

①下列有关说法不正确的是_______________
A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在1L密闭容器中充入3molH2和1 molCO2发生反应I,250℃时反应的平衡常数K=__________(保留3位小数);若要进一步提高甲醇体积分数,可采取的措施有__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应,前后均可以用同一个离子方程式表示的是
A.HCl+Na2CO3 HCl+NaHCO3
B.HCl+Na2CO3 H2SO4+K2CO3
C.H2S+NaOH H2SO4+KOH
D.BaCl2+Na2SO4 BaCO3+H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在某一容积为2 L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:

回答下列问题:
①该反应的化学方程式为__________________________________。
②前2 min用A的浓度变化表示的化学反应速率为________。在2 min时,图像发生改变的原因是________(填字母)。
A.增大压强 B.降低温度 C.加入催化剂 D.增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/mol·L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
①该反应的化学方程式________________________________,达到平衡时四氧化二氮的转化率为_______。
②在0~20 s内,四氧化二氮的平均反应速率为______,哪一时间段______(指0~20、20~40、40~60、60~80、80~100 s)反应速率最大并解释______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学设计实验探究碳、硅元素的非金属性的相对强弱,实验装置如图。根据要求完成下列各题。
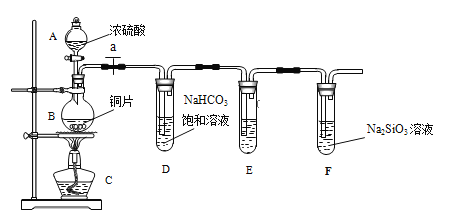
(1)填写所示仪器名称:A__________,B__________。
(2)实验步骤:连接仪器、______________、加药品后,打开 a、滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是________________________________;装置E中装的是酸性KMnO4溶液,其作用是_____________________________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________________。
③依据试管 D 中的反应,能否证明S的非金属性强于C的非金属性___(填 “能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As的原子结构示意图为![]() ,下列关于As的描述不正确的是 ( )
,下列关于As的描述不正确的是 ( )
A. 位于第四周期,第ⅤA族 B. 属于非金属元素
C. 酸性:H3AsO4﹥H3PO4 D. 稳定性:AsH3﹤PH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com