
| A、0.225mol/L |
| B、0.15mol/L |
| C、0.35mol/L |
| D、0.45mol/L |
| m |
| M |
| n |
| V |
| 1.92g |
| 64g/mol |
| 3 |
| 8 |
| 0.0225mol |
| 0.1L |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:

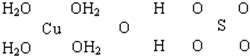

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等 |
| B、加压,V正、V逆 都增大,且V正 增大的倍数大于V逆增大的倍数 |
| C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆减小的倍数 |
| D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数;化学平衡正移,N2 转换率增大,H2转化率也增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
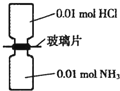 室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( )
室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( )| A、反应前气体的总体积为0.448L |
| B、装置中氢元素的总质量为0.04g |
| C、生成物中含有0.01NA个分子 |
| D、生成物完全溶于水后所得溶液含有0.01 NA个NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体 | B、悬浊液 |
| C、乳浊液 | D、溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com