
| 3 |
| 4 |
| A、2:1 | B、3:2 |
| C、1:1 | D、2:3 |
| ||
| ||
| 1 |
| 4 |
| ||
| x |
| 2 |
| ||
| ||
| 3 |
| 4 |
| 3 |
| 4 |
| 1 |
| 4 |
| ||
| x |
| 2 |
| x |
| 2 |
| x |
| 2 |
| ||
| x+y |
| 1 |
| 4 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C、浓H2SO4有强氧化性,但不能与Cu发生反应 |
| D、SO2具有还原性,故可作漂白剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
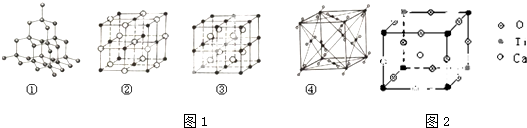
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
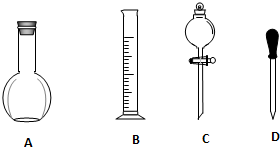
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 温度/℃ | 加入某盐 | H2SO4体积/mL | H2O体积/mL | 铝粉加入量/g | 铝粉溶解量/g |
| ① | 20 | 不加 | 40 | 0 | 2.0050 | 0.0307 |
| ② | 80 | 不加 | 40 | 0 | 2.0050 | 0.1184] |
| ③ | t1 | 不加 | 20 | V1 | 2.0050 | ﹨ |
| ④ | t2 | 5mL0.01mol?L-1 CuSO4溶液 | 20 | V2 | 2.0050 | ﹨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、未加入稀盐酸之前c( CN-)>c(HCN) | ||
B、加稀盐酸后溶液中
| ||
| C、pH=7时,溶液中c( Na+)=c( CN-) | ||
| D、加稀盐酸后HCN的电离程度减小,但c( H+)增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com