
(1)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
①黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,氧化产物为________,若有3 mol FeS2参加反应,转移________mol电子。
6SO2+Fe3O4,氧化产物为________,若有3 mol FeS2参加反应,转移________mol电子。
②与明矾相似,硫酸铁也可用作净水剂,其原理为_______________________________
____________(用离子方程式表示)。
③FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为____________________。
(2)已知:S2O 有较强的还原性,实验室可用I-测定K2S2O8样品的纯度,反应方程式为
有较强的还原性,实验室可用I-测定K2S2O8样品的纯度,反应方程式为
S2O +2I-===2SO
+2I-===2SO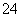 +I2①
+I2①
I2+2S2O ===2I-+S4O
===2I-+S4O ②
②
S2O 、S4O
、S4O 、I2氧化性强弱顺序:______________________。
、I2氧化性强弱顺序:______________________。
(3)已知溶液中,还原性为HSO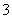 >I-,氧化性为IO
>I-,氧化性为IO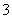 >I2>SO
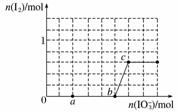
>I2>SO 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
①a点处的还原产物是__________(填离子符号);
b点→c点反应的离子方程式是_________________________________。
②当溶液中的I-为0.5 mol时,加入的KIO3可能是________ mol。
答案 (1)①SO2、Fe3O4 32
②Fe3++3H2OFe(OH)3(胶体)+3H+
③2Fe3++2I-===2Fe2++I2
(2)S2O >I2>S4O
>I2>S4O
(3)①I- IO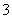 +6H++5I-===3H2O+3I2
+6H++5I-===3H2O+3I2
②0.5或1.1
解析 (1)①根据O2计算转移电子数,若有3 mol FeS2参加反应,则有8 mol O2得电子,应转移32 mol电子。
③氧化性Fe3+>I2,所以FeCl3与HI反应的离子方程式为2Fe3++2I-===2Fe2++I2。
(2)根据氧化剂氧化性大于氧化产物氧化性可以判断氧化性S2O >I2>S4O
>I2>S4O 。
。
(3)反应原理为IO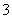 +3HSO
+3HSO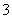 ===I-+3SO
===I-+3SO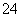 +3H+,IO
+3H+,IO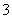 +5I-+6H+===3I2+3H3O。
+5I-+6H+===3I2+3H3O。
①a点IO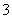 被还原成I-。
被还原成I-。
②a.当有1.5 mol HSO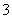 反应时,
反应时,
IO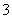 + 3HSO
+ 3HSO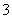 ===I-+3SO
===I-+3SO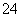 +3H+
+3H+
0.5 mol 1.5 mol 0.5 mol
此时加入KIO3为0.5 mol;
b.IO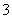 + 3HSO
+ 3HSO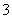 ===I-+3SO
===I-+3SO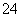 +3H+
+3H+
1 mol 3 mol 1 mol
5I- + IO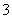 +6H+===3I2+3H2O
+6H+===3I2+3H2O
1 mol-0.5 mol 0.1 mol
=0.5 mol
加入的KIO3为1.1 mol。


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
用铁制备较纯净的三氧化二铁,下列实验方案最好的是( )
A.使铁在潮湿的空气中缓慢氧化
B.铁在氯气中燃烧,加水溶解,加入足量NaOH溶液,过滤、洗涤、然后充分加热分解
C.使铁溶解于稀硫酸,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
D.使铁与足量稀硝酸反应,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)100 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,生成的氯气的物质的量小于0.3 mol,为什么?
(2)将一Cu片投入稀H2SO4溶液中,没观察到反应现象,然后向其中加入少量的KNO3晶体,看到溶液由无色逐渐变蓝并有少量气泡产生,为什么?
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在铜的冶炼过程中有如下反应发生
5FeS2+14CuSO4+12H2O===7Cu2S+5FeSO4+12H2SO4
关于此反应,下列说法正确的是( )
A.Cu2S既是氧化产物,又是还原产物
B.5 mol FeS2发生反应,有10 mol电子转移
C.FeS2只作还原剂
D.产物中的SO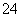 有一部分是氧化产物
有一部分是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)____S+____KOH===____K2S+____K2SO3+____H2O
(2)____P4+____KOH+____H2O===____K3PO4+____PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO2气体和672 mL的N2O4气体(都已折算到标准状态),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于( )
A.8.64 B.9.20
C.9.00 D.9.44
查看答案和解析>>
科目:高中化学 来源: 题型:
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是_______________________________。
(2)将MnO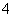 氧化Fe2+的离子方程式补充完整:
氧化Fe2+的离子方程式补充完整:
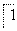 MnO
MnO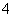 +
+ Fe2++
Fe2++ ________===
________===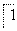 Mn2++
Mn2++ Fe3++
Fe3++ ________。
________。
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的___________________________。
(4)已知:一定条件下,MnO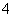 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是_____________________________。
②Ⅳ中加入MnSO4的目的是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分子或离子在指定的分散系中能大量共存的一组是( )
A.银氨溶液:Na+、K+、NO 、NH3·H2O
、NH3·H2O
B.空气:C2H2、CO2、SO2、NO
C.氢氧化铁胶体:H+、K+、S2-、Br-
D.高锰酸钾溶液:H+、Na+、SO 、葡萄糖分子
、葡萄糖分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com