

分析 (1)由N2(g)+3H2(g)?2NH3(g),则反应的平衡常数K=$\frac{c{\;}^{2}(NH{\;}_{3})}{c(N{\;}_{2})c{\;}^{3}(H{\;}_{2})}$;
(2)分析图象变化量,压缩体积,增大压强,平衡向正反应移动,改变瞬间n(N2)不变,达平衡是n(N2)减小;
(3)图3表示平衡时氨气含量与氢气起始物质的量关系,曲线上各点都处于平衡状态,达平衡后,增大氢气用量,氮气的转化率增大.
解答 解:(1)N2(g)+3H2(g)?2NH3(g),反应的平衡常数K=$\frac{c{\;}^{2}(NH{\;}_{3})}{c(N{\;}_{2})c{\;}^{3}(H{\;}_{2})}$,故答案为:K=$\frac{c{\;}^{2}(NH{\;}_{3})}{c(N{\;}_{2})c{\;}^{3}(H{\;}_{2})}$;
(2)从11min起其它条件不变,压缩容器的体积为1L,压强增大,平衡正向进行,瞬间氮气物质的量不变,随平衡正向进行,氮气物质的量减小,则n(N2)的变化曲线d符合;故答案为:d;
(3)图3表示平衡时氨气含量与氢气起始物质的量关系,曲线上各点都处于平衡状态,故a、b、c都处于平衡状态,达平衡后,增大氢气用量,氮气的转化率增大,故a、b、c三点中,c的氮气的转化率最高;
故答案为:c.
点评 本题考查了化学反应和化学平衡影响因素的分析判断,图象分析和平衡常数变化是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①③ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应过程中,分子的种类一定发生改变 | |
| B. | 已知2A(g)+B(g)?C(g)+D(s)△H<0,则该反应一定能自发进行 | |
| C. | 有化学键发生断裂,就有化学反应的发生 | |
| D. | 放热反应的反应速率一定比吸热反应的反应速率大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2mol CO+0.5mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1.5mol CO+0.5mol H2O(g)+0.4mol CO2+0.4mol H2 | |
| C. | 1mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| D. | 0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铝片插入硝酸汞溶液中:Al+Hg2+=Al3++Hg | |
| C. | Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 盐酸除铁锈:O2-+2H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
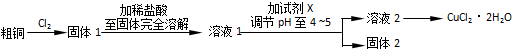
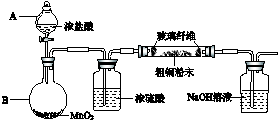
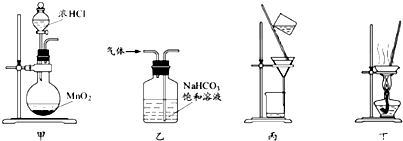
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com